由于格式問題此試題可能會出現亂碼的情況
為了方便您閱讀請點擊右上角的全屏查看
2018眉山市中考化學模擬試題
一、選擇題(本大題共32分)
1.在我們的日常生活中涉及到許多變化,下列變化中不包含化學變化的是( )
A.用石灰漿涂抹墻壁后,表面有水珠生成
B.在口中咀嚼米飯或饅頭時感到有甜味
C.用干冰做制冷劑進行人工降雨
D.使用煤氣作燃料燒飯做菜
2.化學是以實驗為基礎的學科,下列有關實驗現象的描述中,正確的是( )
A.電解水實驗中正極與負極產生的氣體體積之比為1:8
B.硫粉在氧氣中燃燒產生藍紫色火焰
C.將鐵絲插入硫酸銅溶液中,鐵絲上會有紅色固體生成,溶液變成無色
D.在氯化銅溶液中滴加氫氧化鈉溶液,有白色沉淀生成
3.下列實驗裝置中不能用來測定空氣中氧氣含量的是( )
A.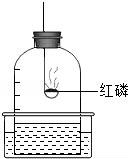 ????????????? B.
????????????? B.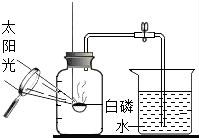 ????????????? C.
????????????? C.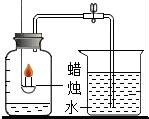 ????????????? D.
????????????? D.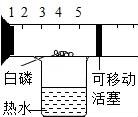
4.在進行“氧氣的實驗室制取與性質”實驗時,某同學制得的氧氣不純.你認為可能的原因是( )
A.用排水法收集時O2 ,集氣瓶裝滿水
B.用向上排空氣法收集O2 時,導管伸入到集氣瓶的底部
C.用排水法收集O2 時,導管口冒出氣泡,立即收集
D.用排水法收集O2 ,收集滿后,在水下蓋上玻璃片
5.下列關于“物質﹣﹣用途﹣﹣性質”的說法不正確的是( )
A.汽油﹣﹣去除油污﹣﹣能乳化油污
B.天然氣﹣﹣用作燃料﹣﹣具有可燃性
C.液氮﹣﹣用作冷凍麻醉劑﹣﹣能氣化吸熱
D.氫氧化鎂﹣﹣治療胃酸過多癥﹣﹣能與胃液中的鹽酸發生中和反應
6.下列反應的化學方程式書寫完全正確的是( )
A.鐵在氧氣中燃燒2Fe+3O2![]() 2Fe2O3
2Fe2O3
B.鹽酸除鐵銹Fe2O3+6HCl═2FeCl3+3H2O
C.密閉容器中燃燒紅磷驗證質量守恒定律2P+O2![]() P2O5
P2O5
D.CO還原氧化鐵Fe2O3+3CO═2Fe+3CO2
7.對下列事實的解釋,不合理的是( )
A.通過氣味辨別氮氣和氨氣 分子是運動的,不同分子的性質不同
B.氧氣經壓縮儲存在鋼瓶中 壓強增大,分子之間的間隔變小
C.干冰升華為二氧化碳氣體 狀態變化,分子大小隨之變化
D.蔗糖在熱水中溶解更快 溫度越高,分子運動速率越大
8.如圖是鈣元素在元素周期表中的信息及鈣原子的原子結構示意圖,下列關于鈣元素的說法錯誤的是( )
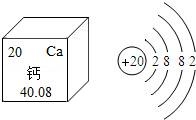
A.核內有20個質子
B.相對原子質量是40.08
C.屬于非金屬元素
D.在化學反應中,鈣原子易失去兩個電子
9.(眉山市中考化學)水是生命之源.下列關于水的說法不正確的是( )
A.水由液態變成氣態時,分子間空隙變大
B.電解水生成氫氣和氧氣,說明水是由氫氣和氧氣組成
C.活性炭具有吸附性,可用于除去水中的異味
D.如果將水樣蒸干后有固體析出,這種水樣中一定含有雜質
10.為提高煤的利用率,可將其轉化為可燃性氣體,此過程可認為是碳與水的反應,微觀示意圖如圖所示,下列說法錯誤的是( )
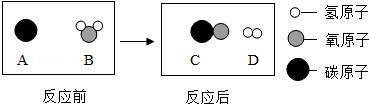
A.生成的兩種物質都屬于單質????????????? B.生成物的分子個數比為1:1
C.分子是由原子結合而成的????????????? D.在化學變化中原子不可分
11.金剛石、石墨和C60的化學性質相似,物理性質卻有很大的差異,其原因是( )
A.金剛石、石墨和C60里碳原子的排列方式不同
B.構成它們的原子數目不同
C.金剛石、石墨和C60由不同種原子構成
D.構成它們的原子大小不同
12.下列曲線能正確表達對應的反應或過程的是( )
A.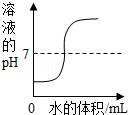
向一定量的鹽酸中逐滴加水稀釋
B.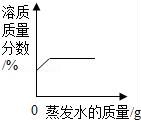
某溫度下將一定量接近飽和的KNO3溶液恒溫蒸發水分
C.
金屬與一定量的稀硫酸反應,由圖象可知,金屬N比金屬M活潑
D.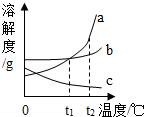
將a、b、c三種物質的飽和溶液分別由t1℃升溫至t2℃時,所得溶液中溶質質量分數大小關系是:a>b>c
13.(眉山市中考化學)如表歸納和總結完全正確的一組是( )
A.化學與生活 | B.化學與安全 |
①用洗滌劑去除油污 ②用醋酸除水垢 ③用食鹽除公路上的積雪 | ①炒菜鍋著火可以用鍋蓋蓋火 ②在室內放一盆水能防止煤氣中毒 ③夜間發現液化氣泄漏開燈尋找泄漏源 |
C.化學與資源 | D.化學與發現 |
①防止金屬腐蝕是保護金屬資源的途徑之一 ②煤、石油、天然氣是可再生能源 ③海洋中蘊藏著豐富的化學資源 | ①波義耳發現酸堿指示劑 ②拉瓦錫發現元素周期律并編制元素周期表 ③門捷列夫發現空氣的組成 |
A.A????????????? B.B????????????? C.C????????????? D.D
14.向硫酸亞鐵、硫酸銅的混合溶液中加入一些鋅粉,充分反應后,過濾,得到濾渣A和濾液.將濾渣A加入少量稀硫酸中,有氣泡產生.以下對濾渣A的組成成分判斷的五種情況,其中合理的有( )
①Cu???? ②Fe、Cu???? ③Zn、Fe???? ④Zn、Cu????? ⑤Zn、Fe、Cu.
A.②⑤????????????? B.②③????????????? C.②③④⑤????????????? D.①②⑤
15.某校化學小組在利用硫酸和氫氧化鈉溶液探究酸堿中和反應時,利用數字化傳感器測得燒杯中溶液pH的變化,其圖象如圖所示,下列說法正確的是( )
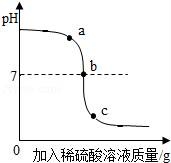
A.圖中c點所示溶液呈堿性
B.圖中a點所示溶液中,含有的溶質是Na2SO4和H2SO4
C.該實驗是將氫氧化鈉溶液逐滴滴入到盛有硫酸的燒杯中
D.由a點到b點的pH變化過程證明酸和堿發生了中和反應
16.某溶液可能含有鹽酸、硫酸、硝酸鈉、氯化銅中的一種或幾種,為了探究其組成,向一定質量的該溶液中逐滴加入氫氧化鋇溶液,生成沉淀的質量與所加氫氧化鋇溶液的質量之間的關系如圖所示,下列相關說法正確的是( )
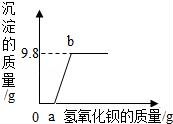
A.加入氫氧化鋇溶液至過量,共發生了三個化學反應
B.該溶液一定含有鹽酸、氯化銅,可能含有硝酸鈉
C.反應過程生成的沉淀一定有氫氧化銅,可能有硫酸鋇
D.到達b點時所消耗氫氧化鋇溶液中溶質的質量是17.1g
二、(眉山市中考化學)填空題(本大題共25分)
17.選用下列物質的序號填空:
①金剛石??? ②一氧化碳??? ③生石灰??? ④石灰石??? ⑤碳酸氫鈉
(1)廣泛用于建筑材料的是 ?? ;
(2)可用于制玻璃刀的材料是 ??
(3)可用于食品干燥劑的是 ?? ;
(4)可用于治療胃酸過多的是 ??
(5)煉鐵時做還原劑的是 ?? .
18.化學是造福人類的科學.
(1)能源化學﹣﹣使用新能源的汽車可節約化石燃料.化石燃料包括煤、天然氣和 ?? ;
(2)農業化學﹣﹣化肥對提高農作物產量具有重要作用.尿素【CO(NH2)2】屬于 ?? (填“氮”、“磷”或“鉀”)肥;
(3)醫藥化學﹣﹣我國藥學家屠呦呦因研制抗瘧新藥青蒿素獲得諾貝爾獎.由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的過程中主要發生了 ?? (填“物理”或“化學”)變化;
(4)材料化學﹣﹣為防止食品變質常采用真空包裝,目的是隔絕 ?? ;檢驗塑料包裝袋是否為熱塑性塑料的方法(包括操作、現象) ?? .
19.某化學興趣小組的同學做粗鹽提純實驗,如圖是同學們作粗鹽提純的實驗示意圖.請回答下列問題:
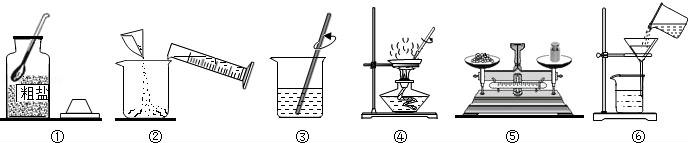
(1)操作③中玻璃棒攪拌的作用是 ?? .
(2)操作⑥中的錯誤是: ?? .
(3)粗鹽提純實驗中的操作順序為 ?? (填操作序號),以及稱量精鹽并計算產率.
(4)操作④中,當觀察到蒸發皿內 ?? 時,停止加熱,讓余熱蒸干剩余液體.
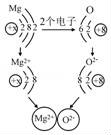
20.如圖是鎂原子和氧原子形成氧化鎂的示意圖
①從得失氧的角度看,鎂與氧氣的反應屬于 ?? 反應;從得失電子的角度看,反應中鎂原子 ?? (填“得到”或“失去”)2個電子,形成相對穩定結構.
②由圖甲可知,元素的原子得到電子后,其化合價將 ?? (填“升高”或“降低”).

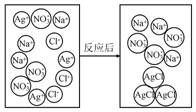
21.如圖是NaCl與AgNO3兩溶液反應的示意圖.
①圖中NO3﹣的名稱是 ?? .
②該反應的本質是 ?? 結合生成沉淀.
③請再用AgNO3作反應物之一,寫出另一個與上述反應本質相同的化學方程式: ?? .
22.物質王國舉行擊鼓傳花的游戲.某學習小組由鐵、氫氣、氧化銅、二氧化碳、稀硫酸、氫氧化鈉、氯化銅七名成員組成.游戲的規則是:相互之間能發生反應就可以進行傳遞.請把上述成員安排在A﹣G的相應位置上,使花束能從A傳到G.其中A為組長,其固體俗稱為干冰.F為副組長,其為黑色固體,請回答:
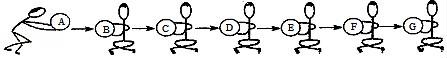
(1)氫氧化鈉應放在位置 ?? 上.
(2)C和D反應的化學方程式為 ?? ,反應類型為 ?? (填基本反應類型).
(3)上述物質除了發生從A到G的化學反應外,常溫下,還能相互發生反應的是: ?? (用化學方程式表示).
(4)當G換成另一個與G同類別的物質時就能將花束傳回起點A,它是 ?? (填物質名稱).
三、實驗探究題(本大題共7分)
23.在學校藥品室發現一卷放置已久的鎂帶,表面有一層白色固體.
提出問題:鎂帶變質了嗎?
查閱資料:鎂久置于潮濕空氣中會變成堿式碳酸鎂[Mg2(OH)2CO3]
ii堿式碳酸鎂和鹽酸反應生成氯化鎂、水、二氧化碳.
iii鎂與冷水不反應.
進行猜想:猜想一:鎂帶沒有變質.
猜想二:鎂帶部分變質生成了堿式碳酸鎂.
猜想三:鎂帶完全變質生成堿式碳酸鎂.
實驗探究:
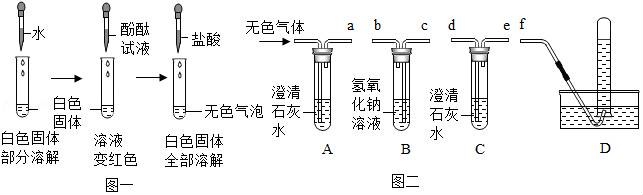
(1)同學們設計了如圖一所示的實驗,根據實驗結果可以否定猜想 ?? (填編號,下同).
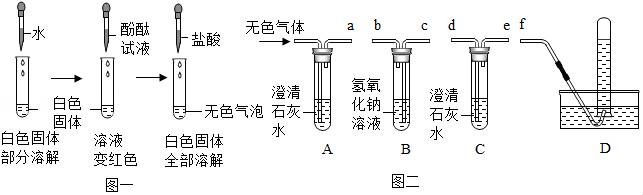
(2)(眉山市中考化學)為了進一步探究另兩種猜想,同學們收集圖一所示實驗中產生的無色氣體,用圖二所示的實驗裝置繼續實驗:
Ⅰ.按ABCD的順序連接好儀器.
Ⅱ.A中有明顯變化,其現象是澄清石灰水變渾濁,反應方程式是 ??
B裝置的作用是 ?? ;C裝置的作用是 ?? .
Ⅲ.C中無明顯變化,若D中收集到無色氣體,則可證明猜想 ?? 成立,D中收集到的氣體是 ?? ;若D中沒有收集到無色氣體,則證明猜想 ?? 成立.
四、計算題(本大題共6分)
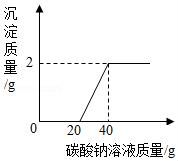
24.實驗小組的同學對實驗室制取二氧化碳反應后的溶液進行了如下探究:取大理石和鹽酸反應且過濾后所得廢液20克于燒杯中,逐滴滴入碳酸鈉溶液至過量,滴入碳酸鈉溶液的質量與生成沉淀的質量的變化關系如圖所示.試回答:
(1)分析圖中信息可知,20g廢液中,所含的溶質是 ?? (寫化學式);
(2)在廢液中加入碳酸鈉溶液,首先與碳酸鈉溶液反應的化學方程式為 ?? ;
(3)計算廢液中氯化鈣的質量分數是多少?(寫出計算過程)
眉山市中考化學參考答案與試題解析
一、選擇題(本大題共32分)
1.在我們的日常生活中涉及到許多變化,下列變化中不包含化學變化的是( )
A.用石灰漿涂抹墻壁后,表面有水珠生成
B.在口中咀嚼米飯或饅頭時感到有甜味
C.用干冰做制冷劑進行人工降雨
D.使用煤氣作燃料燒飯做菜
【考點】E3:化學變化和物理變化的判別.
【分析】化學變化是指有新物質生成的變化,物理變化是指沒有新物質生成的變化,化學變化和物理變化的本質區別是否有新物質生成;據此分析判斷.
【解答】解:A、用石灰漿涂抹墻壁后,表面有水珠生成過程中有新物質生成,屬于化學變化.
B、在口中咀嚼米飯或饅頭時感到有甜味過程中有新物質生成,屬于化學變化.
C、用干冰做制冷劑進行人工降雨過程中只是狀態發生改變,沒有新物質生成,屬于物理變化.
D、使用煤氣作燃料燒飯做菜過程中有新物質生成,屬于化學變化.
故選C.
2.化學是以實驗為基礎的學科,下列有關實驗現象的描述中,正確的是( )
A.電解水實驗中正極與負極產生的氣體體積之比為1:8
B.硫粉在氧氣中燃燒產生藍紫色火焰
C.將鐵絲插入硫酸銅溶液中,鐵絲上會有紅色固體生成,溶液變成無色
D.在氯化銅溶液中滴加氫氧化鈉溶液,有白色沉淀生成
【考點】95:堿的化學性質;6A:氧氣與碳、磷、硫、鐵等物質的反應現象;71:電解水實驗;85:金屬的化學性質.
【分析】A、根據電解水的實驗現象,進行分析判斷.
B、根據硫粉在氧氣中燃燒的現象,進行分析判斷.
C、根據金屬的化學性質,進行分析判斷.
D、根據堿的化學性質,進行分析判斷.
【解答】解:A、電解水實驗中正極與負極產生的氣體體積之比為1:2,故選項說法錯誤.
B、硫粉在氧氣中燃燒產生藍紫色火焰,故選項說法正確.
C、將鐵絲插入硫酸銅溶液中,生成硫酸亞鐵溶液和銅,鐵絲上會有紅色固體生成,溶液變成淺綠色,故選項說法錯誤.
D、在氯化銅溶液中滴加氫氧化鈉溶液,生成氫氧化銅沉淀和氯化鈉,會觀察到有藍色沉淀生成,故選項說法錯誤.
故選:B.
3.下列實驗裝置中不能用來測定空氣中氧氣含量的是( )
A. ????????????? B.
????????????? B.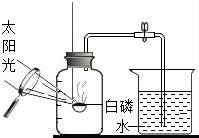 ????????????? C.
????????????? C.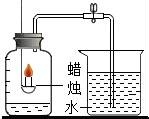 ????????????? D.
????????????? D.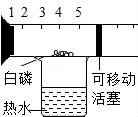
【考點】62:空氣組成的測定.
【分析】本題是測定空氣中氧氣的含量,我們常用燃燒紅磷或白磷的方法,因為磷燃燒生成白色固體五氧化二磷,幾乎不占空間,使得內外產生氣壓差,從而得到正確的結論.因此在選擇可燃物時,必須考慮到:燃燒的條件;生成物的狀態;不與空氣中其他物質發生反應.
【解答】解:A、紅磷燃燒生成白色固體五氧化二磷,幾乎不占空間,使得內外產生氣壓差,正確;
B、白磷燃燒生成白色固體五氧化二磷,使得內外產生氣壓差,水會倒流,正確;
C、蠟燭燃燒生成的是二氧化碳,二氧化碳是氣體,占了氧氣的空間,水幾乎不進入,錯誤;
D、白磷燃燒生成白色固體五氧化二磷,幾乎不占空間,使得內外產生氣壓差,正確;
故選C.
4.(眉山市中考化學)在進行“氧氣的實驗室制取與性質”實驗時,某同學制得的氧氣不純.你認為可能的原因是( )
A.用排水法收集時O2 ,集氣瓶裝滿水
B.用向上排空氣法收集O2 時,導管伸入到集氣瓶的底部
C.用排水法收集O2 時,導管口冒出氣泡,立即收集
D.用排水法收集O2 ,收集滿后,在水下蓋上玻璃片
【考點】6G:制取氧氣的操作步驟和注意點.
【分析】根據制取氧氣時的實驗過程及注意事項分析.
【解答】解:
A、用排水法收集,集氣瓶中裝滿水,可以把集氣瓶中的空氣排盡,故正確;
B、用排空氣法收集氧氣,導氣管伸到集氣瓶的底部,可以把集氣瓶中的空氣排盡,故正確;
C、用排水法收集,沒有等到氣泡連續均勻放出時就開始收集,原試管內的空氣進入集氣瓶,故錯誤;
D、用排水法收集O2 ,收集滿后,在水下蓋上玻璃片,可以防止空氣的進入,故正確.
答案:C
5.下列關于“物質﹣﹣用途﹣﹣性質”的說法不正確的是( )
A.汽油﹣﹣去除油污﹣﹣能乳化油污
B.天然氣﹣﹣用作燃料﹣﹣具有可燃性
C.液氮﹣﹣用作冷凍麻醉劑﹣﹣能氣化吸熱
D.氫氧化鎂﹣﹣治療胃酸過多癥﹣﹣能與胃液中的鹽酸發生中和反應
【考點】7A:溶解現象與溶解原理;6K:常見氣體的用途;97:中和反應及其應用;H3:常用燃料的使用與其對環境的影響.
【分析】A、汽油除油污利用的溶解原理.
B、根據天然氣的可燃性分析.
C、根據三態轉化與吸放熱關系分析.
D、根據中和原理分析.
【解答】解:A、汽油除油污利用的溶解原理,不是乳化原理,故錯誤;
B、天然氣具有可燃性,可用作燃料,故正確;
C、液氮汽化能吸熱,可用作冷凍麻醉劑,故正確;
D、氫氧化鎂能與胃液中的鹽酸發生中和反應,可以治療胃酸過多,故正確.
故選:A.
6.下列反應的化學方程式書寫完全正確的是( )
A.鐵在氧氣中燃燒2Fe+3O2![]() 2Fe2O3
2Fe2O3
B.鹽酸除鐵銹Fe2O3+6HCl═2FeCl3+3H2O
C.密閉容器中燃燒紅磷驗證質量守恒定律2P+O2![]() P2O5
P2O5
D.CO還原氧化鐵Fe2O3+3CO═2Fe+3CO2
【考點】G5:書寫化學方程式、.
【分析】化學方程式的書寫要注意以下幾個方面:①反應是否符合客觀事實,②是否已配平,③條件和符號是否漏缺,④化學式書寫是否錯誤.
【解答】解:A、生成物錯誤,鐵在氧氣中燃燒生成四氧化三鐵,正確的方程式為:3Fe+2O2![]() Fe3O4,故A錯誤;
Fe3O4,故A錯誤;
B、應用的原理正確,化學式書寫正確,也滿足質量守恒定律,故B正確;
C、方程式的書寫需要進行配平,正確的方程式為:4P+5O2![]() 2P2O5,故C錯誤,
2P2O5,故C錯誤,
D、缺少反應條件,正確的方程式為:Fe2O3+3CO![]() 2Fe+3CO2,故D錯誤,
2Fe+3CO2,故D錯誤,
故選B
7.對下列事實的解釋,不合理的是( )
A.通過氣味辨別氮氣和氨氣 分子是運動的,不同分子的性質不同
B.氧氣經壓縮儲存在鋼瓶中 壓強增大,分子之間的間隔變小
C.干冰升華為二氧化碳氣體 狀態變化,分子大小隨之變化
D.蔗糖在熱水中溶解更快 溫度越高,分子運動速率越大
【考點】B9:利用分子與原子的性質分析和解決問題.
【分析】根據分子的基本特征:分子質量和體積都很小;分子之間有間隔;分子是在不斷運動的;同種的分子性質相同,不同種的分子性質不同,可以簡記為:“兩小運間,同同不不”,結合事實進行分析判斷即可.
【解答】解:A、通過氣味辨別氮氣和氨氣,是因為分子是早不斷的運動的,且不同種的分子性質不同,故選項解釋正確.
B、氧氣經壓縮儲存在鋼瓶中,是因為分子間有間隔,氣體受壓后,分子間隔變小,氣體的體積減小,故選項解釋正確.
C、干冰升華為二氧化碳氣體,是因為狀態變化,分子間的間隔隨之變化,故選項解釋錯誤.
D、蔗糖在熱水中溶解更快,是因為溫度越高,分子運動速率越快,故選項解釋正確.
故選:C.
8.如圖是鈣元素在元素周期表中的信息及鈣原子的原子結構示意圖,下列關于鈣元素的說法錯誤的是( )

A.核內有20個質子
B.相對原子質量是40.08
C.屬于非金屬元素
D.在化學反應中,鈣原子易失去兩個電子
【考點】(眉山市中考化學)C5:元素周期表的特點及其應用;B8:原子結構示意圖與離子結構示意圖.
【分析】A、根據原子結構示意圖中,圓圈內數字表示核內質子數,進行分析判斷.
B、圖中元素周期表可以獲得的信息:漢字下面的數字表示相對原子質量,進行分析判斷.
C、金屬元素名稱一般有“钅”字旁,進行分析判斷.
D、原子結構示意圖中,弧線表示電子層,弧線上的數字表示該層上的電子數,若原子的最外層電子數≥4,在化學反應中易得電子,若最外層電子數<4,在化學反應中易失去電子.
【解答】解:A、由鈣原子的原子結構示意圖,圓圈內數字表示核內質子數,核內有20個質子,故選項說法正確.
B、由圖中元素周期表可以獲得的信息,漢字下面的數字表示相對原子質量,相對原子質量是40.08,故選項說法正確.
C、鈣帶“钅”字旁,屬于金屬元素,故選項說法錯誤.
D、鈣原子的最外層電子數為2,在化學反應中易失去兩個電子,故選項說法正確.
故選:C.
9.水是生命之源.下列關于水的說法不正確的是( )
A.水由液態變成氣態時,分子間空隙變大
B.電解水生成氫氣和氧氣,說明水是由氫氣和氧氣組成
C.活性炭具有吸附性,可用于除去水中的異味
D.如果將水樣蒸干后有固體析出,這種水樣中一定含有雜質
【考點】71:電解水實驗;BA:分子的定義與分子的特性;C6:碳單質的物理性質及用途.
【分析】根據水組成、電解水試驗的現象和結論、水的凈化等分析判斷.
【解答】解:A、水由液態變成氣態時,分子間空隙變大,故A說法正確;
B、電解水生成氫氣和氧氣,說明水是由氫元素和氧元素組成,故B說法不正確;
C、活性炭具有吸附性,可用于除去水中的異味,故C說法正確;
D、如果將水樣蒸干后有固體析出,這種水樣中一定含有雜質,故D說法正確.
故選B.
10.為提高煤的利用率,可將其轉化為可燃性氣體,此過程可認為是碳與水的反應,微觀示意圖如圖所示,下列說法錯誤的是( )

A.生成的兩種物質都屬于單質????????????? B.生成物的分子個數比為1:1
C.分子是由原子結合而成的????????????? D.在化學變化中原子不可分
【考點】B3:微粒觀點及模型圖的應用;A7:單質和化合物的判別;B5:分子和原子的區別和聯系.
【分析】根據反應的微觀示意圖書寫化學方程式,根據方程式的意義分析判斷有關的問題.
【解答】解:由反應的微觀示意圖可知,該反應的化學方程式為:C+H2O ![]() CO+H2.
CO+H2.
A、由方程式可知,生成的兩種物質中有一種屬于單質,故A錯誤;
B、由方程式可知,生成物的分子個數比為1:1,故B正確;
C、分子是由原子結合而成的,故C正確;
D、由微粒的變化可知,在化學變化中原子不可分,故D正確.
故選A.
11.金剛石、石墨和C60的化學性質相似,物理性質卻有很大的差異,其原因是( )
A.金剛石、石墨和C60里碳原子的排列方式不同
B.構成它們的原子數目不同
C.金剛石、石墨和C60由不同種原子構成
D.構成它們的原子大小不同
【考點】C6:碳單質的物理性質及用途.
【分析】根據金剛石、石墨、C60的構成可知,由于原子排列不同,彼此間物理性質有差異,它們是由同種的碳原子構成,原子的大小相同,組成元素相同.
【解答】解:因為構成金剛石、石墨、C60的碳原子的排列方式不同,導致物理性質有很大差異.所以A正確,B、C、D錯誤.
故選A.
12.下列曲線能正確表達對應的反應或過程的是( )
A.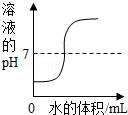
向一定量的鹽酸中逐滴加水稀釋
B.
某溫度下將一定量接近飽和的KNO3溶液恒溫蒸發水分
C.
金屬與一定量的稀硫酸反應,由圖象可知,金屬N比金屬M活潑
D.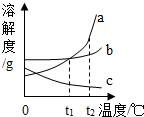
將a、b、c三種物質的飽和溶液分別由t1℃升溫至t2℃時,所得溶液中溶質質量分數大小關系是:a>b>c
【考點】(眉山市中考化學)97:中和反應及其應用;7R:溶質的質量分數;7T:溶質的質量分數、溶解性和溶解度的關系;85:金屬的化學性質;99:溶液的酸堿性與pH值的關系.
【分析】A、根據酸在稀釋過程中,pH值不斷增加,但是pH值不會大于7進行分析;
B、根據某溫度下將一定量接近飽和的KNO3溶液恒溫蒸發水分,溶質質量分數不斷壯增大,然后不變進行分析;
C、根據金屬活動性順序進行分析;
D、根據將a、b、c三種物質的飽和溶液分別由t1℃升溫至t2℃時,a、b物質的溶解度增大,不會析出晶體,c物質的溶解度減小,會析出晶體進行分析.
【解答】解:A、酸在稀釋過程中,pH值不斷增加,但是pH值不會大于7,故A錯誤;
B、某溫度下將一定量接近飽和的KNO3溶液恒溫蒸發水分,溶質質量分數不斷壯增大,然后不變,故B正確;
C、金屬與一定量的稀硫酸反應,由圖象可知,金屬M比金屬N活潑,故C錯誤;
D、將a、b、c三種物質的飽和溶液分別由t1℃升溫至t2℃時,a、b物質的溶解度增大,c物質的溶解度減小,會析出晶體,所得溶液中溶質質量分數大小關系是:a=b>c,故D錯誤.
故選:B.
13.如表歸納和總結完全正確的一組是( )
A.化學與生活 | B.化學與安全 |
①用洗滌劑去除油污 ②用醋酸除水垢 ③用食鹽除公路上的積雪 | ①炒菜鍋著火可以用鍋蓋蓋火 ②在室內放一盆水能防止煤氣中毒 ③夜間發現液化氣泄漏開燈尋找泄漏源 |
C.化學與資源 | D.化學與發現 |
①防止金屬腐蝕是保護金屬資源的途徑之一 ②煤、石油、天然氣是可再生能源 ③海洋中蘊藏著豐富的化學資源 | ①波義耳發現酸堿指示劑 ②拉瓦錫發現元素周期律并編制元素周期表 ③門捷列夫發現空氣的組成 |
A.A????????????? B.B????????????? C.C????????????? D.D
【考點】9G:常用鹽的用途;51:化學的歷史發展過程;7H:乳化現象與乳化作用;8I:金屬資源的保護;93:酸的化學性質;H4:滅火的原理和方法;H5:防范爆炸的措施;HC:海洋中的資源;HO:常見能源的種類、能源的分類.
【分析】A、根據物質的性質和作用進行分析判斷;
B、根據物質的性質及安全常識進行分析判斷;
C、根據資源的保護和利用方法分析判斷;
D、根據各科學家的發現進行分析判斷
【解答】解:A、①洗滌劑具有乳化作用,常用洗滌劑去除油污;②食醋可以與水垢反應,用醋酸除水垢;③食鹽溶液的凝固點較低,用食鹽除公路上的積雪;故選項化學知識歸納正確;
B、①炒菜鍋著火可以用鍋蓋蓋火,正確;②在室內放一盆水,不能防止煤氣中毒,因為一氧化碳不溶于水;③夜間發現液化氣泄漏開燈尋找泄漏源,易發生爆炸,故選項化學知識歸納有錯誤;
C、①防止金屬腐蝕是保護金屬資源的途徑之一;②煤、石油、天然氣是不可再生能源,錯誤;③海洋中蘊藏著豐富的化學資源,故選項化學知識歸納有錯誤;
D、門捷列夫發現元素周期律并編制元素周期表,拉瓦錫發現空氣的組成.故選項化學知識歸納有錯誤;
故選:A.
14.向硫酸亞鐵、硫酸銅的混合溶液中加入一些鋅粉,充分反應后,過濾,得到濾渣A和濾液.將濾渣A加入少量稀硫酸中,有氣泡產生.以下對濾渣A的組成成分判斷的五種情況,其中合理的有( )
①Cu???? ②Fe、Cu???? ③Zn、Fe???? ④Zn、Cu????? ⑤Zn、Fe、Cu.
A.②⑤????????????? B.②③????????????? C.②③④⑤????????????? D.①②⑤
【考點】85:金屬的化學性質.
【分析】根據金屬活動性順序表進行分析.在金屬活動性順序中,排在氫前面的金屬能與酸反應生成氫氣,位置在前的金屬能將位于其后的金屬從其鹽溶液中置換出來.
【解答】解:根據金屬活動順序表可知,鋅比鐵活潑,鐵比銅活潑.所以,加入一定量的鋅粉,首先鋅粉和硫酸銅溶液反應,置換出單質銅,如果鋅粉足量可以繼續與硫酸亞鐵反應置換出鐵.由題意可知,向濾出的固體中滴加稀硫酸,有氣泡產生,說明固體中含有和稀硫酸反應的金屬,由題可知,金屬可能是鐵或鐵和鋅.則濾渣A的組成成分可能為Fe、Cu;Zn、Fe、Cu.
故選A.
15.某校化學小組在利用硫酸和氫氧化鈉溶液探究酸堿中和反應時,利用數字化傳感器測得燒杯中溶液pH的變化,其圖象如圖所示,下列說法正確的是( )
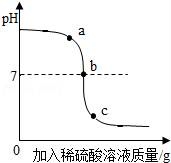
A.圖中c點所示溶液呈堿性
B.圖中a點所示溶液中,含有的溶質是Na2SO4和H2SO4
C.該實驗是將氫氧化鈉溶液逐滴滴入到盛有硫酸的燒杯中
D.由a點到b點的pH變化過程證明酸和堿發生了中和反應
【考點】97:中和反應及其應用;99:溶液的酸堿性與pH值的關系.
【分析】A、根據c點的pH小于7,溶液顯酸性,據此進行分析判斷.
B、根據a點的pH大于7,溶液顯堿性,據此進行分析判斷.
C、根據圖象中pH值的變化是從大于7逐漸的減小到小于7,進行分析解答.
D、根據由a到b點的pH值的變化是從大于7逐漸的減小到等于7,進行分析解答.
【解答】解:A、c點的pH小于7,溶液顯酸性,故錯誤;
B、a點的pH大于7,溶液顯堿性,溶液中的溶質是硫酸鈉和氫氧化鈉,故錯誤;
C、由圖象可知,pH值是開始時大于7逐漸的減小到7然后小于7,可知原溶液顯堿性,然后不斷的加入酸性溶液,使pH減小,說明是把稀鹽酸滴加到氫氧化鈉溶液中,故錯誤;
D、由a到b點的pH值的變化是從大于7逐漸的減小到等于7,可以說明酸和堿發生了中和反應,故正確.
答案:D
16.(眉山市中考化學)某溶液可能含有鹽酸、硫酸、硝酸鈉、氯化銅中的一種或幾種,為了探究其組成,向一定質量的該溶液中逐滴加入氫氧化鋇溶液,生成沉淀的質量與所加氫氧化鋇溶液的質量之間的關系如圖所示,下列相關說法正確的是( )
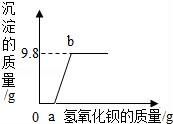
A.加入氫氧化鋇溶液至過量,共發生了三個化學反應
B.該溶液一定含有鹽酸、氯化銅,可能含有硝酸鈉
C.反應過程生成的沉淀一定有氫氧化銅,可能有硫酸鋇
D.到達b點時所消耗氫氧化鋇溶液中溶質的質量是17.1g
【考點】95:堿的化學性質;93:酸的化學性質;9H:鹽的化學性質;G6:根據化學反應方程式的計算.
【分析】由題目的信息和圖象可知:沉淀開始時沒有產生,說明原溶液中有酸,因為硫酸與氫氧化鋇反應生成硫酸鋇白色沉淀,硫酸鋇不溶于三大強酸,因此有鹽酸,沒有硫酸;氯化銅與氫氧化鋇能產生氫氧化銅藍色沉淀,并且符合題意,因此一定有氯化銅,而硝酸鈉不能確定.
【解答】解:由圖象可知一開始加入氫氧化鋇,沒有沉淀,反應一段時間后又產生了沉淀,說明肯定有一種物質能與氫氧化鋇產生沉淀,一開始不產生沉淀是因為其中含有酸,酸能把產生的沉淀溶解,所以加入的氫氧化鋇先與酸反應,把酸反應完了再與另一種物質反應生成沉淀,酸不能是稀硫酸,硫酸與氫氧化鋇反應生成硫酸鋇沉淀,不溶于酸所以圖象中的沉淀應該從原點開始,所以只能是鹽酸,所以與氫氧化鋇產生沉淀只能是氯化銅溶液了,所以該混合物組成一定含有鹽酸和氯化銅溶液,可能含有硝酸鈉.
A、加入氫氧化鋇溶液至過量,共發生了兩個化學反應,一是鹽酸和氫氧化鋇反應生成氯化鋇和水,二是氯化銅和氫氧化鋇反應生成氫氧化銅藍色沉淀和氯化鋇,故A錯誤;
B、由上述分析可知該溶液一定含有鹽酸、氯化銅,可能含有硝酸鈉,故B正確;
C、由上述分析可知反應過程生成的沉淀一定有氫氧化銅,一定沒有硫酸鋇,故C錯誤;
D、到達b點時,由于鹽酸的質量不知道,所以鹽酸消耗的氫氧化鋇無法計算,故不能消耗氫氧化鋇溶液中溶質的質量,故D錯誤.
故選:B.
二、填空題(本大題共25分)
17.選用下列物質的序號填空:
①金剛石??? ②一氧化碳??? ③生石灰??? ④石灰石??? ⑤碳酸氫鈉
(1)廣泛用于建筑材料的是 ④ ;
(2)可用于制玻璃刀的材料是 ①
(3)可用于食品干燥劑的是 ③ ;
(4)可用于治療胃酸過多的是 ⑤
(5)煉鐵時做還原劑的是 ② .
【考點】9G:常用鹽的用途;8B:鐵的冶煉;8L:生石灰的性質與用途;C6:碳單質的物理性質及用途.
【分析】物質的性質決定物質的用途,根據已有的物質的性質進行分析解答即可.
【解答】解:(1)石灰石廣泛用于建筑材料;
(2)金剛石硬度大,可用于制玻璃刀;
(3)生石灰吸水,可用于食品干燥劑;
(4)可用于治療胃酸過多的是碳酸氫鈉;
(5)一氧化碳具有還原性,煉鐵時做還原劑.
故填:(1)④;(2)①;(3)③;(4)⑤;(5)②.
18.化學是造福人類的科學.
(1)能源化學﹣﹣使用新能源的汽車可節約化石燃料.化石燃料包括煤、天然氣和 石油 ;
(2)農業化學﹣﹣化肥對提高農作物產量具有重要作用.尿素【CO(NH2)2】屬于 氮 (填“氮”、“磷”或“鉀”)肥;
(3)醫藥化學﹣﹣我國藥學家屠呦呦因研制抗瘧新藥青蒿素獲得諾貝爾獎.由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的過程中主要發生了 化學 (填“物理”或“化學”)變化;
(4)材料化學﹣﹣為防止食品變質常采用真空包裝,目的是隔絕 氧氣 ;檢驗塑料包裝袋是否為熱塑性塑料的方法(包括操作、現象) 取樣,灼燒,看塑料是否熔化 .
【考點】I1:塑料及其應用;9J:常見化肥的種類和作用;E3:化學變化和物理變化的判別;H6:燃燒、爆炸、緩慢氧化與自燃;H7:化石燃料及其綜合利用.
【分析】(1)根據化石燃料的分類進行分析;
(2)根據化肥的分類進行分析;
(3)根據化學變化和物理變化的本質區別是否有新物質生成進行分析;
(4)根據食品腐敗的原因進行分析;根據熱塑性塑料的特性進行分析.
【解答】解:(1)化石燃料包括煤、天然氣、石油.故填:石油.
(2)含有氮元素的肥料稱為氮肥,尿素中含有氮元素,是一種氮肥.故填:氮.
(3)由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的過程中有新物質生成,屬于化學變化.故填:化學.
(4)食品變質的主要原因是食品與氧氣發生緩慢氧化的結果,所以真空包裝的目的是除去空氣,防止食品發生氧化而變質;檢驗塑料包裝袋是否為熱塑性塑料的方法是:取樣,灼燒,看塑料是否熔化.故填:氧氣、取樣,灼燒,看塑料是否熔化.
19.(眉山市中考化學)某化學興趣小組的同學做粗鹽提純實驗,如圖是同學們作粗鹽提純的實驗示意圖.請回答下列問題:
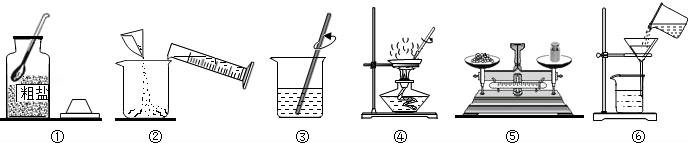
(1)操作③中玻璃棒攪拌的作用是 加快粗鹽的溶解速率 .
(2)操作⑥中的錯誤是: 缺少玻璃棒引流 .
(3)粗鹽提純實驗中的操作順序為 ①⑤②③⑥④ (填操作序號),以及稱量精鹽并計算產率.
(4)操作④中,當觀察到蒸發皿內 出現較多量的固體 時,停止加熱,讓余熱蒸干剩余液體.
【考點】9E:氯化鈉與粗鹽提純;4I:蒸發與蒸餾操作.
【分析】(1)操作③是溶解操作,結合玻璃棒的作用,進行分析解答.
(2)操作⑥是過濾操作,過濾液體時,注意“一貼、二低、三靠”的原則.
(3)根據粗鹽提純是將粗鹽中含有的泥沙等不溶物除去,進行分析解答.
(4)根據蒸發操作中停止加熱的時機,進行分析解答.
【解答】解:(1)操作③是溶解操作,玻璃棒攪拌的作用是加快粗鹽的溶解速率.
(2)操作⑥是過濾操作,過濾液體時,注意“一貼、二低、三靠”的原則,圖中缺少玻璃棒引流.
(3)粗鹽的主要成分是氯化鈉,粗鹽提純是通過溶解(把不溶物與食鹽初步分離)、過濾(把不溶物徹底除去)、蒸發(食鹽從溶液中分離出來而得到食鹽的過程)、稱量精鹽、計算產率,操作步驟的先后順序是①⑤②③⑥④.
(4)蒸發時,待蒸發皿中出現較多量的固體時,應停止加熱,利用余熱將剩余液體蒸干.
故答案為:(1)加快粗鹽的溶解速率;(2)缺少玻璃棒引流;(3)①⑤②③⑥④;(4)出現較多量的固體時.
20.如圖是鎂原子和氧原子形成氧化鎂的示意圖
①從得失氧的角度看,鎂與氧氣的反應屬于 氧化反應 反應;從得失電子的角度看,反應中鎂原子 失去 (填“得到”或“失去”)2個電子,形成相對穩定結構.
②由圖甲可知,元素的原子得到電子后,其化合價將 降低 (填“升高”或“降低”).
【考點】B6:原子和離子的相互轉化.
【分析】①根據有氧參加的反應叫氧化反應,鎂原子最外層有兩個電子,容易失去兩個電子形成穩定結構進行分析;
②根據原子得到電子后質子數不變,電子數增加,所以形成的離子帶負電,化合價降低進行分析;
【解答】解:
①有氧參加的反應叫氧化反應,所以鎂與氧氣的反應屬于氧化反應,鎂原子最外層有兩個電子,容易失去兩個電子形成穩定結構;
②原子得到電子后質子數不變,電子數增加,所以形成的離子帶負電,化合價降低;
答案:①氧化﹣還原;失去;②降低;
21.如圖是NaCl與AgNO3兩溶液反應的示意圖.
①圖中NO3﹣的名稱是 硝酸根 .
②該反應的本質是 Ag+和Cl﹣ 結合生成沉淀.
③請再用AgNO3作反應物之一,寫出另一個與上述反應本質相同的化學方程式: AgNO3+HCl=AgCl↓+HNO3 .

【考點】9H:鹽的化學性質;G5:書寫化學方程式、.
【分析】①根據常見的酸根離子的名稱進行分析;
②根據反應的微觀過程示意圖,從構成從微觀粒子的角度分析該反應酸與堿中和的實質;
③根據硝酸銀與可溶性的氯化物反應實質都為銀離子和氯根離子生成氯化銀沉淀進行分析.
【解答】解:①圖中NO3﹣的名稱是硝酸根;
②由反應的微觀過程示意圖,該反應的實質是銀離子和氯離子生成氯化銀沉淀;
③硝酸銀與可溶性的氯化物反應實質都為銀離子和氯根離子生成氯化銀沉淀,鹽酸和硝酸銀反應生成氯化銀沉淀和硝酸,化學方程式為:AgNO3+HCl=AgCl↓+HNO3.
故答案為:①硝酸根;
②Ag+和Cl﹣;
③AgNO3+HCl=AgCl↓+HNO3.
22(眉山市中考化學).物質王國舉行擊鼓傳花的游戲.某學習小組由鐵、氫氣、氧化銅、二氧化碳、稀硫酸、氫氧化鈉、氯化銅七名成員組成.游戲的規則是:相互之間能發生反應就可以進行傳遞.請把上述成員安排在A﹣G的相應位置上,使花束能從A傳到G.其中A為組長,其固體俗稱為干冰.F為副組長,其為黑色固體,請回答:
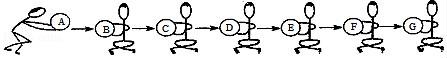
(1)氫氧化鈉應放在位置 B 上.
(2)C和D反應的化學方程式為 CuCl2+Fe=FeCl2+Cu ,反應類型為 置換反應 (填基本反應類型).
(3)上述物質除了發生從A到G的化學反應外,常溫下,還能相互發生反應的是: 2NaOH+H2SO4=Na2SO4+2H2O (用化學方程式表示).
(4)當G換成另一個與G同類別的物質時就能將花束傳回起點A,它是 碳 (填物質名稱).
【考點】AE:物質的鑒別、推斷;85:金屬的化學性質;93:酸的化學性質;95:堿的化學性質;9H:鹽的化學性質;FA:反應類型的判定;G5:書寫化學方程式、.
【分析】根據鐵、氫氣、氧化銅、二氧化碳、硫酸、氫氧化鈉、氯化銅之間的兩兩反應關系及相互之間能發生反應就可以進行傳遞的條件進行大膽的假設,最后能夠符合傳遞的要求即可.
【解答】解:A的固體俗稱干冰,因此A是二氧化碳,二氧化碳能夠和氫氧化鈉反應,則B是氫氧化鈉;氫氧化鈉能夠和硫酸和氯化銅反應,假設C是氯化銅,氯化銅能夠和鐵反應,因此D就是鐵;鐵能夠和硫酸反應,因此E就是硫酸;硫酸能夠和氧化銅反應,氧化銅能夠和氫氣反應,因此F是氧化銅,G是氫氣,帶入驗證符合要求,因此:
(1)氫氧化鈉能夠和二氧化碳反應,因此氫氧化鈉在B位置上;故填:B;
(2)C是氯化銅,D是鐵,鐵和氯化銅反應產生氯化亞鐵和銅;該反應是單質和化合物生成新的單質和化合物的置換反應;故填:Fe+CuCl2=FeCl2+Cu;置換反應;
(3)常溫下硫酸能與氫氧化鈉反應,化學方程式為:H2SO4+2NaOH=Na2SO4+2H2O;故填:H2SO4+2NaOH=Na2SO4+2H2O;
(3)G是氫氣,氫氣和碳都能夠還原氧化銅,因此可以把氫氣換成碳;故填:碳.
三、實驗探究題(本大題共7分)
23.在學校藥品室發現一卷放置已久的鎂帶,表面有一層白色固體.
提出問題:鎂帶變質了嗎?
查閱資料:鎂久置于潮濕空氣中會變成堿式碳酸鎂[Mg2(OH)2CO3]
ii堿式碳酸鎂和鹽酸反應生成氯化鎂、水、二氧化碳.
iii鎂與冷水不反應.
進行猜想:猜想一:鎂帶沒有變質.
猜想二:鎂帶部分變質生成了堿式碳酸鎂.
猜想三:鎂帶完全變質生成堿式碳酸鎂.
實驗探究:
(1)同學們設計了如圖一所示的實驗,根據實驗結果可以否定猜想 一 (填編號,下同).
(2)為了進一步探究另兩種猜想,同學們收集圖一所示實驗中產生的無色氣體,用圖二所示的實驗裝置繼續實驗:
Ⅰ.按ABCD的順序連接好儀器.
Ⅱ.A中有明顯變化,其現象是澄清石灰水變渾濁,反應方程式是 Ca(OH)2+CO2═CaCO3↓+H2O
B裝置的作用是 除去二氧化碳氣體 ;C裝置的作用是 檢驗二氧化碳氣體是否除盡 .
Ⅲ.C中無明顯變化,若D中收集到無色氣體,則可證明猜想 二 成立,D中收集到的氣體是 氫氣 ;若D中沒有收集到無色氣體,則證明猜想 三 成立.
【考點】26:藥品是否變質的探究;4Q:常見氣體的檢驗與除雜方法;85:金屬的化學性質;9H:鹽的化學性質;G5:書寫化學方程式、.
【分析】(1)因為鎂與冷水不反應,白色固體能夠部分溶解,說明猜想一不正確;
(2)二氧化碳能使澄清石灰水變渾濁,是因為二氧化碳能和氫氧化鈣反應生成碳酸鈣沉淀和水;
氫氧化鈉溶液能夠吸收二氧化碳氣體;
鎂能和稀鹽酸反應生成氯化鎂和氫氣.
【解答】解:(1)如圖一所示的實驗,白色固體部分溶解,說明鎂已經變質,即猜想一不正確.
故填:一.
(2)Ⅱ.A中有明顯變化,其現象是澄清石灰水變渾濁,說明無色氣體中含有二氧化碳,二氧化碳和氫氧化鈣反應生成了碳酸鈣和水,反應方程式是:Ca(OH)2+CO2═CaCO3↓+H2O;
B裝置的作用是除去二氧化碳氣體;
C裝置的作用是檢驗二氧化碳氣體是否除盡.
故填:Ca(OH)2+CO2═CaCO3↓+H2O;除去二氧化碳氣體;檢驗二氧化碳氣體是否除盡.
Ⅲ.C中無明顯變化,若D中收集到無色氣體,則可證明猜想二成立,D中收集到的氣體是鎂和稀鹽酸反應生成的氫氣;
若D中沒有收集到無色氣體,則證明猜想三成立.
故填:二;氫氣;三.
四、計算題(本大題共6分)
24.實驗小組的同學對實驗室制取二氧化碳反應后的溶液進行了如下探究:取大理石和鹽酸反應且過濾后所得廢液20克于燒杯中,逐滴滴入碳酸鈉溶液至過量,滴入碳酸鈉溶液的質量與生成沉淀的質量的變化關系如圖所示.試回答:
(1)分析圖中信息可知,20g廢液中,所含的溶質是 CaCl2和HCl (寫化學式);
(2)在廢液中加入碳酸鈉溶液,首先與碳酸鈉溶液反應的化學方程式為 Na2CO3+2HCl═2NaCl+CO2↑+H2O ;
(3)計算廢液中氯化鈣的質量分數是多少?(寫出計算過程)

【考點】G6:根據化學反應方程式的計算;7U:有關溶質質量分數的簡單計算.
【分析】(1)根據大理石與稀鹽酸反應生成氯化鈣和水和二氧化碳,產生沉淀前消耗20g碳酸鈉溶液,這是與廢液中剩余鹽酸反應的碳酸鈉溶液的質量,鹽酸與碳酸鈉反應生成氯化鈉、水和二氧化碳;
加入碳酸鈉溶液20g﹣40g時,這是與廢液中氯化鈣與碳酸鈉反應生成碳酸鈣沉淀和氯化鈉;
(2)產生沉淀前消耗20g碳酸鈉溶液,這是與廢液中剩余鹽酸反應的碳酸鈉溶液的質量,鹽酸與碳酸鈉反應生成氯化鈉、水和二氧化碳;
(3)由沉淀質量,根據碳酸鈉與氯化鈣反應的化學方程式可以計算出氯化鈣的質量即可解答;
【解答】(眉山市中考化學)解:(1)大理石與稀鹽酸反應生成氯化鈣和水和二氧化碳;產生沉淀前消耗20g碳酸鈉溶液,這是與廢液中剩余鹽酸反應的碳酸鈉溶液的質量,鹽酸與碳酸鈉反應生成氯化鈉、水和二氧化碳;
加入碳酸鈉溶液20g﹣40g時,這是與廢液中氯化鈣與碳酸鈉反應生成碳酸鈣沉淀和氯化鈉;故20g廢液中,所含的溶質是氯化氫和氯化鈣;
(2)產生沉淀前消耗20g碳酸鈉溶液,這是與廢液中剩余鹽酸反應的碳酸鈉溶液的質量,鹽酸與碳酸鈉反應生成氯化鈉、水和二氧化碳;
(3)設廢液中氯化鈣的質量為x.
Na2CO3+CaCl2═CaCO3↓+2NaCl
????????????? 111?????? 100?????
??????????????? x????????? 2g???????
![]()
x=2.22g,
廢液中氯化鈣的質量分數是:![]() ×100%=11.1%
×100%=11.1%
故答案為:
(1)CaCl2和HCl;
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)廢液中氯化鈣的質量分數是11.1%.

孔乙己是貧困潦倒的知識分子。在書中,孔乙己是一個知識分子,滿口“之乎者也”,但是他很窮,還竊書,說過“讀書人的事,怎么能叫竊,”被人嘲笑,他...

自然界產生氧氣的化學方程式:光合作用的反應式為6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反應和暗反應兩個過程。需要具備光...

有的高校沒有條件,只要學業水平成績都合格就可以,比如中國科學院大學。有的需要平常學習考試成績,比如北京外國語大學要求高三第一學期期末成績在全...

在四則運算中,表示計算順序,在小括號之后、大括號之前;表示兩個整數的最小公倍數;表示取未知數的整數部分;在函數中,表示函數的閉區間;在線性代...

濟南開設的最好的職高學校有:濟南方信集團職業高中、濟南公共交通職業高中。濟南市公共交通職業高級中學是由濟南市公共交通總公司承辦,業務屬濟南市...

實然:是說事物實際上就是這樣的,但不同于現實性(現實性指其有合理性和客觀性);應然:就是應該是怎么樣的意思,比如說這件事,就應該是那樣的結果...

地中海氣候一種夏季炎熱干燥、冬季溫和多雨,雨熱不同期的氣候類型。地中海氣候冬季受西風帶控制,鋒面氣旋頻繁活動,氣候溫和,最冷月的氣溫在4-1...

堿石灰,又稱鈉石灰,堿石灰是白色或米黃色粉末,疏松多孔,是氧化鈣(CaO,大約75%),水(H?O,大約20%),氫氧化鈉(NaOH,大約3...