2018年珠海市中學(xué)中考化學(xué)模擬試題【解析版含答案】
由于版式的問題,試題可能會(huì)出現(xiàn)亂碼的現(xiàn)象,為了方便您的閱讀請(qǐng)點(diǎn)擊全屏查看
一、化學(xué)選擇題(本大題包括14小題,每小題2分,共28分,每小題只有一個(gè)正確選項(xiàng).)
1.遠(yuǎn)到恒星、行星,近到樹木、花草,物質(zhì)世界一刻不停地發(fā)生著變化.下列過程發(fā)生了化學(xué)變化的是()
①烘烤食物
②瓷碗碎了?
③鋼鐵生銹?
④沙子變成沙雕?
⑤干冰升華
⑥擦燃一根火柴??
⑦化石燃料的形成.
A.①③⑥⑦????????????? B.①③④⑥????????????? C.②⑤⑥????????????? D.①③④⑤⑥⑦
2.廣泛用于制造日常生活用品,且地殼中含量最多的金屬元素是()
A.鋁????????????? B.鎂????????????? C.硅????????????? D.鐵
3.從分子的角度分析并解釋如表事實(shí),不正確的是()
選項(xiàng) | 事實(shí) | 解釋 |
A | 碘酒是混合物 | 由不同種分子構(gòu)成 |
B | 端午時(shí)節(jié)粽飄香 | 分子在不斷運(yùn)動(dòng)著 |
C | 氣體受熱膨脹 | 溫度升高,分子自身體積增大 |
D | 固體碘受熱升華 | 碘分子間的間隔變大 |
A.A????????????? B.B????????????? C.C????????????? D.D
4.“以崇尚科學(xué)為榮,以愚昧無知為恥”.下列敘述缺乏科學(xué)依據(jù)的是()
A.不可用工業(yè)酒精勾兌飲用酒
B.用碳酸氫鈉可除去面團(tuán)發(fā)酵產(chǎn)生的酸
C.熟石灰可用于中和酸化的土壤
D.小孩經(jīng)常咬鉛筆芯,會(huì)導(dǎo)致鉛中毒
5.下列方框中符合2H2意義的示意圖是()
A.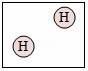 ????????????? B.
????????????? B.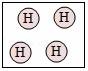 ????????????? C.
????????????? C.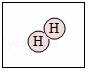 ????????????? D.
????????????? D.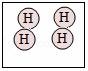
6.成語“釜底抽薪”包含著滅火的原理.下列滅火方法也依據(jù)這個(gè)原理的是()
①熄滅酒精燈時(shí),用燈帽蓋滅;②熄滅燃?xì)庠罨鹧鏁r(shí),關(guān)閉閥門;③用嘴吹滅蠟燭;④森林著火時(shí),將大火蔓延線路前的一片樹木砍掉;⑤房屋著火時(shí),用高壓水槍滅火.
A.①和②????????????? B.②和③????????????? C.②和④????????????? D.①和⑤
7.下列實(shí)驗(yàn)操作正確的是()
A. 二氧化碳驗(yàn)滿????????????? B.
二氧化碳驗(yàn)滿????????????? B.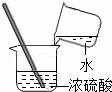 稀釋濃硫酸
稀釋濃硫酸
C.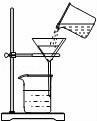 過濾????????????? ??? D.
過濾????????????? ??? D.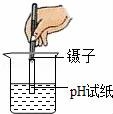 測(cè)定溶液的酸堿度
測(cè)定溶液的酸堿度
8.推理是化學(xué)學(xué)習(xí)中常用的思維方法.下列推理正確的是()
A.蔗糖的飽和溶液,不能再溶解蔗糖,也一定不能再溶解其他物質(zhì)
B.酸和堿能發(fā)生中和反應(yīng),則硝酸與氫氧化鈉也能發(fā)生中和反應(yīng)
C.堿溶液能使石蕊溶液變藍(lán),則能使石蕊溶液變藍(lán)的溶液一定是堿溶液
D.鋁表面的氧化鋁薄膜能起到保護(hù)作用,則鐵表面的鐵銹也能起到保護(hù)作用
9.現(xiàn)有20℃時(shí)NH4Cl飽和溶液200g,今欲改變?cè)擄柡腿芤褐腥苜|(zhì)的質(zhì)量分?jǐn)?shù),可采取的措施是()
A.保持溫度不變,蒸發(fā)掉20g水
B.保持溫度不變,加入20g水
C.保持溫度不變,取出20g溶液
D.保持溫度不變,加入20gNH4Cl固體
10.如圖所示:若關(guān)閉Ⅱ閥打開I閥,紫色小花(用石蕊溶液染成)變紅;若關(guān)閉I閥打開Ⅱ閥,紫色小花不變紅.則甲瓶中所盛的試劑可能是()
①濃硫酸 ②濃NaOH溶液 ③飽和NaCl溶液.
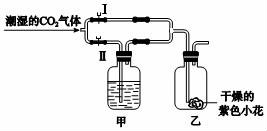
A.只有①????????????? B.①②????????????? C.只有②????????????? D.①②③
11.某溫度時(shí),向一定量的飽和氫氧化鈣溶液中加入少量生石灰,再恢復(fù)到原溫,下列各相關(guān)的變化圖象正確的是()
A.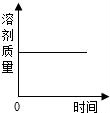 ????????????? B.
????????????? B.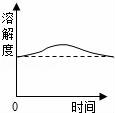 ????????????? C.
????????????? C.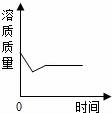 ????????????? D.
????????????? D.
12.分離下列各組混合物,其操作包括溶解、過濾、結(jié)晶三個(gè)步驟的是()
A.氯化鉀和二氧化錳????????????? B.氯化鈉和硝酸鉀
C.氧化鐵和氧化鋁????????????? D.硝酸銅和氫氧化鈉
13.“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的“侯氏制堿法”的重要反應(yīng).如圖是4位同學(xué)對(duì)該反應(yīng)涉及的有關(guān)知識(shí)發(fā)表的部分見解.其中不正確的是()
A. ?????????????
?????????????
B. ?????????????
?????????????
C. ?????????????
?????????????
D.
14.向AgNO3、Cu(NO3)2的混合溶液中加入一定量的鋅粉,充分反應(yīng)后過濾,向?yàn)V液中滴加稀鹽酸有白色沉淀產(chǎn)生.下列說法中,正確的是()
A.所得濾渣中可能含有銅和鋅
B.所得濾渣中一定含有銀和銅
C.所得濾液中可能含有Cu2+
D.所得濾液中一定含有Ag+、Zn2+、Cu2+
二、填空題(共25分)
15.化學(xué)就在我們身邊,它與我們的生活息息相關(guān).請(qǐng)從氯化鈉、硫酸亞鐵、硝酸鋅、鹽酸、硫酸、碳酸氫鈉這幾種物質(zhì)中,選擇適當(dāng)物質(zhì)的化學(xué)式填空:
(1)生活中最常用的調(diào)味品是,
(2)人體胃液中含有的酸是,
(3)治療胃酸過多的藥物小蘇打,
(4)溶液有顏色的是.
16.2015年9月28日,美國(guó)航天局向全世界宣布了“火星有水”的證據(jù),這意味著今天的火星不是我們想象的死寂星球,而是有生命存在的可能.
(1)下列“水”屬于純凈物的是(填序號(hào));
A.海水?? B.河水?? C.自來水?? D.蒸餾水
(2)用下圖裝置進(jìn)行電解水的實(shí)驗(yàn),可用檢驗(yàn)a中氣體,水的電解實(shí)驗(yàn)證明了水是由組成的;
(3)我省粵北地區(qū)部分農(nóng)村用地下水作為生活用水,人們常用檢驗(yàn)地下水是硬水還是軟水,生活中可用的方法降低水的硬度并殺滅病菌.

17.我國(guó)新版《生活飲用水衛(wèi)生標(biāo)準(zhǔn)》(簡(jiǎn)稱新國(guó)標(biāo))中水質(zhì)檢測(cè)指標(biāo)從原來的35項(xiàng)增加到106項(xiàng),對(duì)供水各環(huán)節(jié)的水質(zhì)提出了相應(yīng)的要求.
Ⅰ.新國(guó)標(biāo)在無機(jī)物指標(biāo)中修訂了鎘、鉛等的限量,這里的鎘、鉛指的是(填序號(hào));
A.原子?????????? B.分子????????? C.元素????????? D.單質(zhì)
Ⅱ.新國(guó)標(biāo)中對(duì)水的pH的規(guī)定為6.5≤pH≤8.5,實(shí)驗(yàn)室用pH試紙測(cè)得自來水的pH=6,說明該自來水顯(填“酸”、“堿”或“中”)性,是否符合新國(guó)標(biāo)(填“是”或“否”);
Ⅲ.新國(guó)標(biāo)中消毒劑由1項(xiàng)增至4項(xiàng),加入了對(duì)用臭氧、二氧化氯和氯胺消毒的規(guī)定.
①臭氧(O3)在消毒過程中轉(zhuǎn)化為氧氣,臭氧轉(zhuǎn)化為氧氣屬于(填“物理”或者“化學(xué)”)變化;
②二氧化氯消毒過程中產(chǎn)生的次氯酸根離子(ClO﹣)也有消毒作用,ClO﹣中氯元素的化合價(jià)為價(jià);
③氯胺(NH2Cl)由(填數(shù)字)種元素組成,用氯胺消毒時(shí),反應(yīng)的化學(xué)方程式是NH2Cl+X═NH3+HClO,其中X的化學(xué)式為.
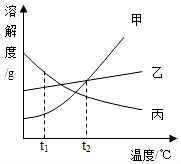
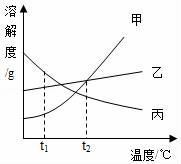
18.如圖是甲、乙、丙三種固體物質(zhì)的溶解度曲線圖,根據(jù)該圖回答下列問題:
(1)t1℃時(shí),三種物質(zhì)的溶解度由大到小的順序是;
(2)將 t2℃時(shí)甲、乙、丙三種物質(zhì)的飽和溶液降溫到t1℃,溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)最大的是,溶質(zhì)的質(zhì)量分?jǐn)?shù)最小的是.
19.元素周期表是學(xué)習(xí)和研究化學(xué)的重要工具,它的內(nèi)容十分豐富.下表是依據(jù)元素周期表畫出的1﹣18號(hào)元素的原子結(jié)構(gòu)示意圖:
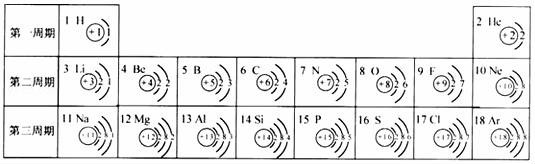
(1)核電荷數(shù)為15的元素名稱是;核電荷數(shù)為9的元素屬于 元素(填“金屬”或“非金屬”),在化學(xué)反應(yīng)中,該元素的原子容易(填“得”或“失”)電子,與該元素化學(xué)性質(zhì)相似的另一元素是(填元素符號(hào));
(2)僅由l、7、8號(hào)元素中的三種組成的一種鹽的化學(xué)式為;
(3)對(duì)1﹣18號(hào)元素的原子結(jié)構(gòu)示意圖進(jìn)行分析,可以發(fā)現(xiàn)許多規(guī)律,如第一周期元素的原子核外只有一個(gè)電子層.請(qǐng)?jiān)倏偨Y(jié)出其它規(guī)律,并寫出其中一條:.
三、簡(jiǎn)答題(共16分)
20.電子工業(yè)常用30%的FeCl3溶液腐蝕覆蓋有一薄層銅的絕緣板,制成印刷電路板.人們?yōu)榱藦膹U腐蝕液(含有CuCl2、FeCl2 和FeCl3)中回收銅,并重新得到FeCl3溶液,設(shè)計(jì)如下實(shí)驗(yàn)流程.
已知:2FeCl3+Fe=3FeCl2

(1)操作 ②、④的名稱是;
(2)上述流程中,X的化學(xué)式為,加入過量的原因是,步驟 ③中有關(guān)反應(yīng)的化學(xué)方程式為;
(3)Z為Cl2,第⑥步發(fā)生的反應(yīng)為化合反應(yīng),此反應(yīng)的化學(xué)方程式為.
21.老師在指導(dǎo)學(xué)生記憶化學(xué)方程式時(shí)指出很多反應(yīng)可以歸納,如:氧化鈣、氫氧化鈣、碳酸鈣等與鹽酸反應(yīng)時(shí)生成物中都含有氯化鈣和水.同學(xué)們興趣很高,也進(jìn)行了歸納:
(1)甲物質(zhì)與稀硫酸反應(yīng)時(shí)生成物中有CuSO4和H2O,則甲物質(zhì)可以是和(請(qǐng)?zhí)顚憙煞N不同類別物質(zhì)的化學(xué)式);寫出上述轉(zhuǎn)化過程中,屬于中和反應(yīng)的化學(xué)方程式.
(2)A﹣H都是初中常見的物質(zhì),其中D為藍(lán)色沉淀,A、E是組成元素相同的兩種氣體,F(xiàn)、H為黑色固體.他們之間轉(zhuǎn)化關(guān)系如圖(反應(yīng)條件及部分反應(yīng)物和生成物已略去)
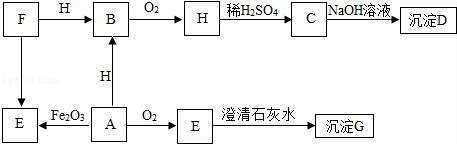
①C的化學(xué)式是;
②寫出反應(yīng)寫出反應(yīng)A![]() E的化學(xué)方程式;
E的化學(xué)方程式;
③寫出反應(yīng)E→G的化學(xué)方程式.
四、實(shí)驗(yàn)題(共20分)
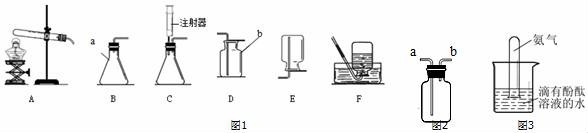
22.如圖1是實(shí)驗(yàn)室常用氣體制備裝置,據(jù)圖回答問題:

(1)請(qǐng)寫出指定儀器的名稱:a,b;
(2)實(shí)驗(yàn)室用高錳酸鉀制氧氣的化學(xué)方程式是,應(yīng)選擇的發(fā)生裝置是(填字母代號(hào)),如果選用圖2裝置收集氧氣,氣體應(yīng)從(填“a”或“b”)端導(dǎo)入;
(3)某化學(xué)小組同學(xué)用20%的過氧化氫溶液和二氧化錳,并選用B裝置來制氧氣,寫出此反應(yīng)的化學(xué)方程式;實(shí)驗(yàn)中,同學(xué)們發(fā)現(xiàn)不能得到平穩(wěn)的氧氣流,大家提出從兩個(gè)方面加以改進(jìn):
一是把發(fā)生裝置由B改為C,其理由是;
二是將過氧化氫溶液加水稀釋,溶液的稀釋需要經(jīng)過計(jì)算、量取、混勻三個(gè)步驟,如果把50g質(zhì)量分?jǐn)?shù)為20%的過氧化氫溶液稀釋成5%的過氧化氫溶液,需加水的質(zhì)量為g,在稀釋過程中,除了燒杯外,還需要用到的儀器有(填數(shù)字序號(hào));
①量筒? ②藥匙?? ③試管?? ④酒精燈? ⑤滴管?? ⑥玻璃棒
(4)實(shí)驗(yàn)室可用加熱氯化銨和熟石灰的固體混合物制取氨氣(NH3),
①制取氨氣應(yīng)選用的裝置是(填字母代號(hào)),
②氨氣極易溶于水,氨水顯堿性.則圖3實(shí)驗(yàn)可觀察到什么現(xiàn)象?.
23.化學(xué)課后,化學(xué)興趣小組的同學(xué)在整理實(shí)驗(yàn)桌時(shí),發(fā)現(xiàn)有一瓶氫氧化鈉溶液沒有塞橡皮塞,征得老師同意后,開展了以下探究:
【提出問題1】該氫氧化鈉溶液是否變質(zhì)了呢?
【實(shí)驗(yàn)探究1】
實(shí)驗(yàn)操作 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
取少量該溶液于試管中,向溶液中滴加稀鹽酸,并不斷振蕩. | 有氣泡冒出. | 氫氧化鈉溶液一定變質(zhì)了. |
【提出問題2】該氫氧化鈉溶液是全部變質(zhì)還是部分變質(zhì)呢?
【猜想與假設(shè)]猜想1:氫氧化鈉溶液部分變質(zhì).? 猜想2:氫氧化鈉溶液全部變質(zhì).
【查閱資料】(1)氯化鈣溶液呈中性.
(2)氯化鈣溶液能與碳酸鈉溶液反應(yīng):CaCl2+Na2CO3═CaCO3↓+2NaCl
【實(shí)驗(yàn)探究2】
實(shí)驗(yàn)步驟 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
(1)取少量該溶液于試管中,向溶液中滴加過量的氯化鈣溶液,并不斷振蕩. | 有生成. | 說明原溶液中一定有碳酸鈉. |
(2)取步驟(1)試管中的少量上層清液,滴加酚酞溶液. | 溶液變紅色. | 說明原溶液中一定有. |
【實(shí)驗(yàn)結(jié)論】該氫氧化鈉溶液(填“部分”或“全部”)變質(zhì).
【反思與評(píng)價(jià)】
(1)氫氧化鈉溶液露置于空氣中容易變質(zhì),請(qǐng)寫出相關(guān)反應(yīng)的化學(xué)方程式:.
(2)在上述【實(shí)驗(yàn)探究2】中,小明提出可用氫氧化鈣溶液代替氯化鈣溶液,你認(rèn)為該方案(填“可行”或“不可行”).
【理解與應(yīng)用】氫氧化鈉溶液容易變質(zhì),必須密封保存.實(shí)驗(yàn)室必須密封保存的藥品還有很多,試另舉一例:.
五、計(jì)算題
24.我國(guó)藥學(xué)家屠呦呦因發(fā)現(xiàn)了治療瘧疾的特效藥青蒿素(挽救了全球數(shù)百萬人的生命)于2015年10月獲得諾貝爾醫(yī)學(xué)獎(jiǎng).她在研究過程中曾關(guān)鍵性地用乙醚提取青蒿素.乙醚的化學(xué)式為C4H10O.請(qǐng)回答:
(1)每個(gè)乙醚分子中有個(gè)原子,乙醚的相對(duì)分子質(zhì)量為;
(2)乙醚(C4H10O)中碳、氧元素質(zhì)量比為;
(3)乙醚(C4H10O)中碳元素的質(zhì)量分?jǐn)?shù)是(精確到0.1%).
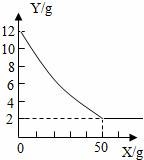
25.銅仁市地處武陵山區(qū),石灰石資源豐富,某課外小組同學(xué)取該樣品12.0g于燒杯中,向盛有樣品的燒杯中加入足量一定溶質(zhì)質(zhì)量分?jǐn)?shù)的稀鹽酸溶液充分反應(yīng),所用稀鹽酸質(zhì)量(用X表示)和燒杯中剩余固體質(zhì)量(用Y表示)如圖所示(石灰石的主要成分是碳酸鈣,雜質(zhì)不溶于水也不與酸反應(yīng)),請(qǐng)回答下列問題:
(1)石灰石中碳酸鈣的質(zhì)量是多少?
(2)充分反應(yīng)后共生成多少二氧化碳?
(3)所用稀鹽酸的溶質(zhì)質(zhì)量分?jǐn)?shù)是多少?
2018年珠海市中學(xué)中考化學(xué)模擬試題參考答案與試題解析
一、選擇題(本大題包括14小題,每小題2分,共28分,每小題只有一個(gè)正確選項(xiàng).)
1.遠(yuǎn)到恒星、行星,近到樹木、花草,物質(zhì)世界一刻不停地發(fā)生著變化.下列過程發(fā)生了化學(xué)變化的是()
①烘烤食物
②瓷碗碎了?
③鋼鐵生銹?
④沙子變成沙雕?
⑤干冰升華
⑥擦燃一根火柴??
⑦化石燃料的形成.
A.①③⑥⑦????????????? B.①③④⑥????????????? C.②⑤⑥????????????? D.①③④⑤⑥⑦
【考點(diǎn)】化學(xué)變化和物理變化的判別.
【專題】物質(zhì)的變化與性質(zhì).
【分析】化學(xué)變化是指有新物質(zhì)生成的變化,物理變化是指沒有新物質(zhì)生成的變化,化學(xué)變化和物理變化的本質(zhì)區(qū)別是否有新物質(zhì)生成;據(jù)此分析判斷.
【解答】解:①烘烤食物 ③鋼鐵生銹? ⑥擦燃一根火柴 ⑦化石燃料的形成等過程中都有新物質(zhì)生成,都屬于化學(xué)變化.
故選A.
【點(diǎn)評(píng)】本題難度不大,解答時(shí)要分析變化過程中是否有新物質(zhì)生成,若沒有新物質(zhì)生成屬于物理變化,若有新物質(zhì)生成屬于化學(xué)變化.
2.廣泛用于制造日常生活用品,且地殼中含量最多的金屬元素是()
A.鋁????????????? B.鎂????????????? C.硅????????????? D.鐵
【考點(diǎn)】地殼中元素的分布與含量.
【專題】結(jié)合課本知識(shí)的信息.
【分析】類似的題目就是要強(qiáng)調(diào)審題,注意題目給定的限制條件,從限制條件去做出問題的判斷.
【解答】解:用途廣泛的且是地殼中含量最多的金屬元素,有時(shí)對(duì)用途廣泛很難以明確的話,從后面的“地殼中含量最多的金屬元素”也可以得出結(jié)論,其實(shí)就是選鋁.所以在學(xué)習(xí)時(shí)要記住地殼中含量前幾位的元素“氧硅鋁鐵”.
故選A.
【點(diǎn)評(píng)】在平時(shí)的學(xué)習(xí)中注意對(duì)一些知識(shí)點(diǎn)的積累,要熟記在心.這樣應(yīng)用起來才方便.
3.從分子的角度分析并解釋如表事實(shí),不正確的是()
選項(xiàng) | 事實(shí) | 解釋 |
A | 碘酒是混合物 | 由不同種分子構(gòu)成 |
B | 端午時(shí)節(jié)粽飄香 | 分子在不斷運(yùn)動(dòng)著 |
C | 氣體受熱膨脹 | 溫度升高,分子自身體積增大 |
D | 固體碘受熱升華 | 碘分子間的間隔變大 |
A.A????????????? B.B????????????? C.C????????????? D.D
【考點(diǎn)】利用分子與原子的性質(zhì)分析和解決問題.
【專題】物質(zhì)的微觀構(gòu)成與物質(zhì)的宏觀組成.
【分析】根據(jù)微粒的特征分析:①體積和質(zhì)量都很小,②微粒之間存在間隔,③微粒是在不斷運(yùn)動(dòng)的,④化學(xué)變化的本質(zhì)是分子分解成原子,原子重新組合成新的分子的過程.
【解答】解:A.碘酒中的溶質(zhì)是碘,碘由碘分子構(gòu)成,酒精是溶劑,酒精是由酒精分子構(gòu)成的,故正確;
B.聞到香味是因?yàn)榉肿釉诓粩嗟倪\(yùn)動(dòng),故正確;
C.氣體受熱膨脹是因?yàn)闅怏w分子間隔變大引起的,故錯(cuò)誤;
D.碘由固態(tài)變?yōu)闅鈶B(tài)是因?yàn)榉肿娱g隔變大引起的,故正確.
故選C.
【點(diǎn)評(píng)】熟練記憶分子和原子的性質(zhì),當(dāng)物質(zhì)發(fā)生物理變化時(shí),構(gòu)成物質(zhì)的分子不發(fā)生變化,大小也不變,改變的是分子間隔,當(dāng)物質(zhì)發(fā)生化學(xué)變化時(shí),構(gòu)成物質(zhì)的分子發(fā)生了變化.
4.“以崇尚科學(xué)為榮,以愚昧無知為恥”.下列敘述缺乏科學(xué)依據(jù)的是()
A.不可用工業(yè)酒精勾兌飲用酒
B.用碳酸氫鈉可除去面團(tuán)發(fā)酵產(chǎn)生的酸
C.熟石灰可用于中和酸化的土壤
D.小孩經(jīng)常咬鉛筆芯,會(huì)導(dǎo)致鉛中毒
【考點(diǎn)】亞硝酸鈉、甲醛等化學(xué)品的性質(zhì)與人體健康;中和反應(yīng)及其應(yīng)用;常用鹽的用途;碳單質(zhì)的物理性質(zhì)及用途.
【專題】化學(xué)知識(shí)生活化;化學(xué)與生活.
【分析】A、根據(jù)甲醇有毒進(jìn)行分析;
B、根據(jù)碳酸氫鈉受熱分解生成二氧化碳?xì)怏w進(jìn)行分析;
C、根據(jù)酸堿中和的知識(shí)進(jìn)行分析;
D、根據(jù)鉛筆芯中含有石墨和粘土,不含有鉛進(jìn)行分析.
【解答】解:A、不可用工業(yè)酒精勾兌飲用酒,因?yàn)楣I(yè)酒精中含有甲醇,甲醇對(duì)人體有害,甚至使人失明,故A正確;
B、碳酸氫鈉受熱分解生成二氧化碳?xì)怏w,使蒸出的饅頭疏松多孔,故B正確;
C、氫氧化鈣具有堿性,且價(jià)格低廉,能與土壤中的酸性物質(zhì)反應(yīng),常用于改良酸性土壤,故C正確;
D、筆芯的成分是石墨和粘土,不含金屬元素鉛,不會(huì)導(dǎo)致鉛中毒,故D錯(cuò)誤;
故選D.
【點(diǎn)評(píng)】解答本題要掌握各種物質(zhì)的性質(zhì)方面的知識(shí),只有這樣才能對(duì)相關(guān)方面的問題做出正確的判斷.
5.下列方框中符合2H2意義的示意圖是()
A. ????????????? B.
????????????? B. ????????????? C.
????????????? C.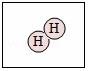 ????????????? D.
????????????? D.
【考點(diǎn)】化學(xué)符號(hào)及其周圍數(shù)字的意義.
【專題】化學(xué)用語和質(zhì)量守恒定律.
【分析】根據(jù)2H2表示2個(gè)氫分子,進(jìn)行分析圖示含義判斷
【解答】解:
A.根據(jù)圖示模型A表示2個(gè)氫原子;故A不符合題意;
B.根據(jù)圖示模型B表示4個(gè)氫原子,故B不符合題意;
C.根據(jù)圖示模型C表示一個(gè)氫分子,故C不符合題意;
D.根據(jù)圖示模型D表示2個(gè)氫分子,故D符合題意;
故選:D
【點(diǎn)評(píng)】本題考查學(xué)生對(duì)化學(xué)式的微觀、宏觀含義的理解與在解題中應(yīng)用的能力.
6.成語“釜底抽薪”包含著滅火的原理.下列滅火方法也依據(jù)這個(gè)原理的是()
①熄滅酒精燈時(shí),用燈帽蓋滅;②熄滅燃?xì)庠罨鹧鏁r(shí),關(guān)閉閥門;③用嘴吹滅蠟燭;④森林著火時(shí),將大火蔓延線路前的一片樹木砍掉;⑤房屋著火時(shí),用高壓水槍滅火.
A.①和②????????????? B.②和③????????????? C.②和④????????????? D.①和⑤
【考點(diǎn)】滅火的原理和方法.
【專題】化學(xué)與能源.
【分析】釜底抽薪體現(xiàn)的是一種常用的滅火方法,它利用的原理是清除可燃物,將鍋底的柴火抽走,就沒有了可燃物,起到滅火的作用.
【解答】解:①燈帽蓋滅酒精燈是隔絕空氣滅火,與“釜底抽薪”滅火原理不同;②熄滅燃?xì)庠罨鹧鏁r(shí),關(guān)閉閥門是移走可燃物滅火,與“釜底抽薪”滅火原理相同;③用嘴吹滅蠟燭是通過降溫至著火點(diǎn)以下來滅火,與“釜底抽薪”滅火原理不同;④砍掉樹木形成隔離帶,可燃物與其他物品隔離,達(dá)到滅火的目的,與“釜底抽薪”滅火原理相同;⑤水滅火是利用降溫至著火點(diǎn)以下來滅火,與“釜底抽薪”滅火原理不同.
故選C.
【點(diǎn)評(píng)】滅火的原理有:(1)清除可燃物或使可燃物與其他物品隔離;(2)隔絕氧氣或空氣;(3)使溫度降到可燃物的著火點(diǎn)以下.
7.下列實(shí)驗(yàn)操作正確的是()
A.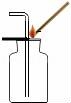 二氧化碳驗(yàn)滿????????????? B.
二氧化碳驗(yàn)滿????????????? B.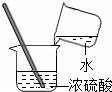 稀釋濃硫酸
稀釋濃硫酸
C.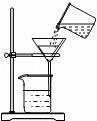 過濾????????????? D.
過濾????????????? D. 測(cè)定溶液的酸堿度
測(cè)定溶液的酸堿度
【考點(diǎn)】溶液的酸堿度測(cè)定;濃硫酸的性質(zhì)及濃硫酸的稀釋;過濾的原理、方法及其應(yīng)用;二氧化碳的檢驗(yàn)和驗(yàn)滿.
【專題】實(shí)驗(yàn)操作型;化學(xué)學(xué)習(xí)中的實(shí)驗(yàn)思想;常見儀器及化學(xué)實(shí)驗(yàn)基本操作.
【分析】A、根據(jù)二氧化碳?xì)怏w的驗(yàn)滿方法進(jìn)行分析判斷.
B、根據(jù)濃硫酸的稀釋方法(酸入水,沿器壁,慢慢倒,不斷攪)進(jìn)行分析判斷.
C、過濾液體時(shí),注意“一貼、二低、三靠”的原則.
D、根據(jù)用pH試紙測(cè)定未知溶液的pH的方法進(jìn)行分析判斷.
【解答】解:A、檢驗(yàn)二氧化碳是否收集滿時(shí),應(yīng)將燃著的木條放在集氣瓶口,圖中所示操作正確.
B、稀釋濃硫酸時(shí),要把濃硫酸緩緩地沿器壁注入水中,同時(shí)用玻璃棒不斷攪拌,以使熱量及時(shí)地?cái)U(kuò)散;一定不能把水注入濃硫酸中;圖中所示操作錯(cuò)誤.
C、過濾液體時(shí),要注意“一貼、二低、三靠”的原則,圖中缺少玻璃棒引流,圖中所示操作錯(cuò)誤.
D、用pH試紙測(cè)定未知溶液的pH時(shí),正確的操作方法為用玻璃棒蘸取少量待測(cè)液滴在干燥的pH試紙上,與標(biāo)準(zhǔn)比色卡對(duì)比來確定pH.不能將pH試紙伸入待測(cè)液中,以免污染待測(cè)液,圖中所示操作錯(cuò)誤.
故選:A.
【點(diǎn)評(píng)】本題難度不大,熟悉各種儀器的用途及使用注意事項(xiàng)、常見化學(xué)實(shí)驗(yàn)基本操作的注意事項(xiàng)是解答此類試題的關(guān)鍵.
8.推理是化學(xué)學(xué)習(xí)中常用的思維方法.下列推理正確的是()
A.蔗糖的飽和溶液,不能再溶解蔗糖,也一定不能再溶解其他物質(zhì)
B.酸和堿能發(fā)生中和反應(yīng),則硝酸與氫氧化鈉也能發(fā)生中和反應(yīng)
C.堿溶液能使石蕊溶液變藍(lán),則能使石蕊溶液變藍(lán)的溶液一定是堿溶液
D.鋁表面的氧化鋁薄膜能起到保護(hù)作用,則鐵表面的鐵銹也能起到保護(hù)作用
【考點(diǎn)】堿的化學(xué)性質(zhì);飽和溶液和不飽和溶液;金屬的化學(xué)性質(zhì);中和反應(yīng)及其應(yīng)用.
【專題】溶液、濁液與溶解度;金屬與金屬材料;常見的酸 酸的通性;常見的堿 堿的通性.
【分析】A、根據(jù)一種物質(zhì)的飽和溶液還能溶解其它物質(zhì),進(jìn)行分析判斷.
B、根據(jù)酸堿能發(fā)生中和反應(yīng),據(jù)此進(jìn)行分析判斷.
C、根據(jù)顯堿性的溶液不一定是堿溶液,進(jìn)行分析判斷.
D、根據(jù)鐵銹很疏松,進(jìn)行分析判斷.
【解答】解:A、一種物質(zhì)的飽和溶液還能溶解其它物質(zhì),蔗糖的飽和溶液,不能再溶解蔗糖,但還能再溶解其他物質(zhì),故選項(xiàng)推理錯(cuò)誤.
B、酸和堿能發(fā)生中和反應(yīng),硝酸與氫氧化鈉分別是酸和堿,也能發(fā)生中和反應(yīng),故選項(xiàng)推理正確.
C、堿溶液能使石蕊溶液變藍(lán),則能使石蕊溶液變藍(lán)的溶液不一定是堿溶液,也可能是碳酸鈉等鹽溶液,故選項(xiàng)推理錯(cuò)誤.
D、鋁表面的氧化鋁薄膜能起到保護(hù)作用,但鐵表面的鐵銹很疏松,不能起到保護(hù)作用,故選項(xiàng)推理錯(cuò)誤.
故選:B.
【點(diǎn)評(píng)】本題難度不大,掌握堿的化學(xué)性質(zhì)、中和反應(yīng)的特征、飽和溶液的特征等并能靈活運(yùn)用是正確解答本題的關(guān)鍵.
9.現(xiàn)有20℃時(shí)NH4Cl飽和溶液200g,今欲改變?cè)擄柡腿芤褐腥苜|(zhì)的質(zhì)量分?jǐn)?shù),可采取的措施是()
A.保持溫度不變,蒸發(fā)掉20g水
B.保持溫度不變,加入20g水
C.保持溫度不變,取出20g溶液
D.保持溫度不變,加入20gNH4Cl固體
【考點(diǎn)】溶質(zhì)的質(zhì)量分?jǐn)?shù).
【專題】溶液、濁液與溶解度.
【分析】A、根據(jù)飽和溶液蒸發(fā)溶劑會(huì)析出晶體,進(jìn)行分析判斷.
B、根據(jù)保持溫度不變,加入20g水后,溶劑的質(zhì)量增加,進(jìn)行分析判斷.
C、根據(jù)溶液具有均一性,進(jìn)行分析判斷.
D、根據(jù)氯化銨的飽和溶液不能繼續(xù)溶解氯化銨,進(jìn)行分析判斷.
【解答】解:A、20℃時(shí)NH4Cl飽和溶液200g,保持溫度不變,蒸發(fā)掉20g水,會(huì)析出晶體,所得溶液仍為該溫度下的飽和溶液,溶質(zhì)的質(zhì)量分?jǐn)?shù)不變,故選項(xiàng)錯(cuò)誤.
B、保持溫度不變,加入20g水后,溶劑的質(zhì)量增加,溶質(zhì)的質(zhì)量不變,則溶質(zhì)的質(zhì)量分?jǐn)?shù)減小,故選項(xiàng)正確.
C、溶液具有均一性,保持溫度不變,取出20g溶液,剩余溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)不變,故選項(xiàng)錯(cuò)誤.
D、氯化銨的飽和溶液不能繼續(xù)溶解氯化銨,保持溫度不變,加入20gNH4Cl固體,氯化銨不溶解,溶質(zhì)的質(zhì)量分?jǐn)?shù)不變,故選項(xiàng)錯(cuò)誤.
故選:B.
【點(diǎn)評(píng)】本題難度不大,理解改變飽和溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)需改變?nèi)芤旱慕M成是正確解答本題的關(guān)鍵.
10.如圖所示:若關(guān)閉Ⅱ閥打開I閥,紫色小花(用石蕊溶液染成)變紅;若關(guān)閉I閥打開Ⅱ閥,紫色小花不變紅.則甲瓶中所盛的試劑可能是()
①濃硫酸 ②濃NaOH溶液 ③飽和NaCl溶液.

A.只有①????????????? B.①②????????????? C.只有②????????????? D.①②③
【考點(diǎn)】二氧化碳的化學(xué)性質(zhì).
【專題】元素與化合物;碳單質(zhì)與含碳化合物的性質(zhì)與用途.
【分析】關(guān)閉Ⅱ閥打開I閥,紫色小花(用石蕊溶液染成)變紅,是因?yàn)槎趸寂c水反應(yīng)生成碳酸,碳酸能使紫色石蕊溶液變紅色;根據(jù)題意,若關(guān)閉I閥打開Ⅱ閥,紫色小花不變紅,說明甲中盛放的試劑能吸收水分或者是能吸收二氧化碳,進(jìn)行分析判斷.
【解答】解:關(guān)閉Ⅱ閥打開I閥,紫色小花(用石蕊溶液染成)變紅,是因?yàn)槎趸寂c水反應(yīng)生成碳酸,碳酸能使紫色石蕊溶液變紅色;若關(guān)閉I閥打開Ⅱ閥,紫色小花不變紅,說明甲中盛放的試劑能吸收水分或者是能吸收二氧化碳,濃硫酸具有吸水性,符合要求;濃氫氧化鈉溶液能吸收二氧化碳,符合要求;飽和NaCl溶液不具有吸水性,不符合要求.
故①②有可能是甲瓶中所盛的試劑.
故選:AB.
【點(diǎn)評(píng)】本題難度不大,熟練掌握二氧化碳與水反應(yīng)生成碳酸、碳酸能使紫色石蕊溶液變紅色、濃硫酸具有吸水性等是正確解答本題的關(guān)鍵.
11.某溫度時(shí),向一定量的飽和氫氧化鈣溶液中加入少量生石灰,再恢復(fù)到原溫,下列各相關(guān)的變化圖象正確的是()
A. ????????????? B.
????????????? B. ????????????? C.
????????????? C. ????????????? D.
????????????? D.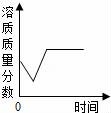
【考點(diǎn)】固體溶解度的概念.
【專題】壓軸實(shí)驗(yàn)題.
【分析】根據(jù)加入少量生石灰后,生石灰與水反應(yīng)生成氫氧化鈣,且放出熱量,溶劑減少溶質(zhì)會(huì)析出一部分來考慮本題.
【解答】解:A、因?yàn)樯遗c水反應(yīng)生成氫氧化鈣,所以溶劑質(zhì)量減少,故A錯(cuò);
B、固體的溶解度影響因素是溫度,由于最后恢復(fù)到原來溫度,所以最后的溶解度與開始時(shí)相等,但由于生石灰與水反應(yīng)放熱,使溫度升高,因?yàn)闅溲趸}的溶解度隨溫度的升高而減小,故B錯(cuò);
C、因?yàn)殚_始生石灰與水反應(yīng)生成氫氧化鈣,所以溶劑質(zhì)量減少,對(duì)于飽和氫氧化鈣溶液來說,溶劑減少就會(huì)析出溶質(zhì),所以溶質(zhì)減少,由于生石灰與水反應(yīng)生成氫氧化鈣時(shí)放出熱量,在反應(yīng)過程中溫度升高,溶解度減小,但冷卻后溫度降低,溶解度又增大了,又溶解了一部分,溫度不變后溶質(zhì)也不變了,故C正確;
D、因?yàn)轱柡腿芤旱馁|(zhì)量分?jǐn)?shù)計(jì)算公式是:![]() ×100%,所以飽和溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)影響因素是溶解度,固體的溶解度影響因素是溫度,由于最后恢復(fù)到原來溫度,所以最后的溶解度與開始時(shí)相等,溶質(zhì)質(zhì)量分?jǐn)?shù)不變,故D錯(cuò).
×100%,所以飽和溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)影響因素是溶解度,固體的溶解度影響因素是溫度,由于最后恢復(fù)到原來溫度,所以最后的溶解度與開始時(shí)相等,溶質(zhì)質(zhì)量分?jǐn)?shù)不變,故D錯(cuò).
故選C.
【點(diǎn)評(píng)】本題容易出錯(cuò)的地方是生石灰與水反應(yīng)生成氫氧化鈣,導(dǎo)致溶劑減少,溶質(zhì)會(huì)析出,仍然飽和,又因?yàn)闇囟炔蛔兯匀苜|(zhì)質(zhì)量分?jǐn)?shù)不變.
12.分離下列各組混合物,其操作包括溶解、過濾、結(jié)晶三個(gè)步驟的是()
A.氯化鉀和二氧化錳????????????? B.氯化鈉和硝酸鉀
C.氧化鐵和氧化鋁????????????? D.硝酸銅和氫氧化鈉
【考點(diǎn)】混合物的分離方法.
【專題】物質(zhì)的分離和提純.
【分析】本題考查混合物分離中的過濾方法,能用溶解、過濾、蒸發(fā)結(jié)晶的步驟分離,則混合物中含不溶性物質(zhì)和可溶性物質(zhì),據(jù)此分析解答即可;
【解答】解:A、氯化鉀是易溶于水的固體,二氧化錳是不溶于水的固體,故可以使用溶解、過濾的方法得到二氧化錳,然后蒸發(fā)濃縮、冷卻結(jié)晶可得到氯化鉀,故A正確;
B、硝酸鉀和氯化鈉都是易溶于水的固體,不能使用過濾的方法分離,故B錯(cuò)誤;
C、氧化鐵和氧化鋁都是不溶于水的固體,不能使用過濾的方法分離,故C錯(cuò)誤;
D、硝酸銅和氫氧化鈉都是能溶于水的固體,不能使用過濾的方法分離,故D錯(cuò)誤.
故選:A.
【點(diǎn)評(píng)】本題考查了混合物的分離,完成此題,可以依據(jù)過濾的原理進(jìn)行,即過濾是能將不溶于液體的固體分離出來的一種方法.
13.“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的“侯氏制堿法”的重要反應(yīng).如圖是4位同學(xué)對(duì)該反應(yīng)涉及的有關(guān)知識(shí)發(fā)表的部分見解.其中不正確的是()
A. ?????????????
?????????????
B. ?????????????
?????????????
C. ?????????????
?????????????
D.
【考點(diǎn)】純堿的制取;飽和溶液和不飽和溶液;常見化肥的種類和作用.
【專題】常見的鹽 化學(xué)肥料.
【分析】A、從“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”可以看出,碳酸氫鈉的溶解度小,以沉淀的形式析出.
B、碳酸氫鈉俗稱小蘇打,碳酸鈉俗稱純堿.
C、析出碳酸氫鈉,說明剩余的溶液為碳酸氫鈉的飽和溶液,據(jù)此進(jìn)行分析判斷.
D、含有氮元素的肥料稱為氮肥,據(jù)此結(jié)合反應(yīng)原理進(jìn)行分析判斷.
【解答】解:A、從“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”可以看出,碳酸氫鈉以沉淀的形式析出,說明碳酸氫鈉的溶解度較小,在該溫度下結(jié)晶析出;故選項(xiàng)說法正確.
B、碳酸氫鈉俗稱小蘇打,不是純堿,故選項(xiàng)說法正確.
C、析出固體后的溶液一定是碳酸氫鈉的飽和溶液,故析出NaHCO3固體后的溶液中還含有碳酸氫鈉,故選項(xiàng)說法錯(cuò)誤.
D、生成的NH4Cl中含有氮元素,屬于氮肥,故選項(xiàng)說法正確.
故選:C.
【點(diǎn)評(píng)】本題難度不大,考查同學(xué)們新信息獲取、處理及靈活運(yùn)用的能力,掌握“侯氏制堿法”的制取原理、飽和溶液等是正確解答本題的關(guān)鍵.
14.向AgNO3、Cu(NO3)2的混合溶液中加入一定量的鋅粉,充分反應(yīng)后過濾,向?yàn)V液中滴加稀鹽酸有白色沉淀產(chǎn)生.下列說法中,正確的是()
A.所得濾渣中可能含有銅和鋅
B.所得濾渣中一定含有銀和銅
C.所得濾液中可能含有Cu2+
D.所得濾液中一定含有Ag+、Zn2+、Cu2+
【考點(diǎn)】金屬的化學(xué)性質(zhì);酸的化學(xué)性質(zhì).
【專題】金屬與金屬材料.
【分析】在金屬活動(dòng)性順序中,氫前的金屬能與酸反應(yīng)生成氫氣,位置在前的金屬能將位于其后的金屬?gòu)钠潲}溶液中置換出來,利用此知識(shí)分析即可.
【解答】解:在金屬活動(dòng)性順序中,鋅>氫>銅>銀,鋅能與硝酸銀反應(yīng)生成銀和硝酸鋅,可以和硝酸銅反應(yīng)生成銅和硝酸鋅;所以放入鋅后鋅要先置換出硝酸銀中銀,再去置換硝酸同種的銅,所以如果向所得濾液中加稀鹽酸有白色沉淀生成,說明溶液中還存在銀離子其白色沉淀是氯化銀,因此硝酸銅一定還沒有反應(yīng),所以濾渣會(huì)是銀不能含有銅和鋅;所以溶液中的金屬陽離子會(huì)有鋅離子和沒有反應(yīng)的銅離子及剩余的銀離子.觀察選項(xiàng),故選項(xiàng)為:D.
【點(diǎn)評(píng)】此題考查了金屬活動(dòng)順序表中鋅、銅、銀的金屬活動(dòng)性強(qiáng)弱,及其金屬活動(dòng)性順序表的應(yīng)用,鍛煉了學(xué)生分析問題解決問題的能力.
二、填空題(共25分)
15.化學(xué)就在我們身邊,它與我們的生活息息相關(guān).請(qǐng)從氯化鈉、硫酸亞鐵、硝酸鋅、鹽酸、硫酸、碳酸氫鈉這幾種物質(zhì)中,選擇適當(dāng)物質(zhì)的化學(xué)式填空:
(1)生活中最常用的調(diào)味品是 NaCl ,
(2)人體胃液中含有的酸是 HCl ,
(3)治療胃酸過多的藥物小蘇打 NaHCO3 ,
(4)溶液有顏色的是 FeSO4 .
【考點(diǎn)】化學(xué)式的書寫及意義.
【專題】化學(xué)用語和質(zhì)量守恒定律.
【分析】首先根據(jù)題意確定物質(zhì)的化學(xué)名稱,然后根據(jù)書寫化學(xué)式的方法和步驟寫出物質(zhì)的化學(xué)式即可.
【解答】解:(1)氯化鈉是生活中常用的調(diào)味品;故填:NaCl;
(2)人體胃液中的酸為鹽酸,可幫助食物的消化;故填:HCl;
(3)小蘇打是碳酸氫鈉的俗稱;故填:NaHCO3;
(4)硫酸亞鐵溶液是淺綠色的;故填:FeSO4.
【點(diǎn)評(píng)】本題難度不大,熟練掌握常見物質(zhì)的性質(zhì)、用途、組成及化學(xué)式的書寫是正確解答此類題的關(guān)鍵所在.
16.2015年9月28日,美國(guó)航天局向全世界宣布了“火星有水”的證據(jù),這意味著今天的火星不是我們想象的死寂星球,而是有生命存在的可能.
(1)下列“水”屬于純凈物的是 D (填序號(hào));
A.海水?? B.河水?? C.自來水?? D.蒸餾水
(2)用下圖裝置進(jìn)行電解水的實(shí)驗(yàn),可用 帶火星的木條 檢驗(yàn)a中氣體,水的電解實(shí)驗(yàn)證明了水是由 氫、氧元素 組成的;
(3)我省粵北地區(qū)部分農(nóng)村用地下水作為生活用水,人們常用 肥皂水 檢驗(yàn)地下水是硬水還是軟水,生活中可用 煮沸 的方法降低水的硬度并殺滅病菌.
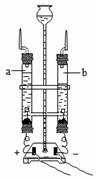
【考點(diǎn)】電解水實(shí)驗(yàn);硬水與軟水;純凈物和混合物的判別.
【專題】空氣與水.
【分析】(1)根據(jù)各種“水”的組成分析類別;
(2)根據(jù)電解水的試驗(yàn)現(xiàn)象、結(jié)論和生成的氣體的性質(zhì)分析回答;
(3)根據(jù)區(qū)別硬水、軟水的方法和生活中硬水軟化的方法分析回答.
【解答】解:(1)在海水、河水、自來水中常含有可溶或不可溶性的雜質(zhì),屬于混合物;蒸餾水是由一種物質(zhì)組成的,屬于純凈物.
(2)由電解水裝置圖可知,a中氣體是電源的正極產(chǎn)生的氣體是氧氣,具有助燃性,可用帶火星的木條檢驗(yàn),水的電解實(shí)驗(yàn)生成了氫氣和氧氣,證明了水是由氫、氧元素 組成的.
(3)我省粵北地區(qū)部分農(nóng)村用地下水作為生活用水,人們常用肥皂水檢驗(yàn)地下水是硬水還是軟水,遇肥皂水產(chǎn)生的泡沫少的是硬水,遇肥皂水產(chǎn)生的泡沫多的是軟水,生活中可用煮沸的方法降低水的硬度并殺滅病菌.
故答為:(1)D;(2)帶火星的木條,氫、氧元素;(3)肥皂水,煮沸.
【點(diǎn)評(píng)】本題主要考查了水的組成、電解和凈化的知識(shí),屬于課本中的基礎(chǔ)知識(shí),加強(qiáng)基礎(chǔ)知識(shí)的學(xué)習(xí),有利于解答本類題.
17.我國(guó)新版《生活飲用水衛(wèi)生標(biāo)準(zhǔn)》(簡(jiǎn)稱新國(guó)標(biāo))中水質(zhì)檢測(cè)指標(biāo)從原來的35項(xiàng)增加到106項(xiàng),對(duì)供水各環(huán)節(jié)的水質(zhì)提出了相應(yīng)的要求.
Ⅰ.新國(guó)標(biāo)在無機(jī)物指標(biāo)中修訂了鎘、鉛等的限量,這里的鎘、鉛指的是 C (填序號(hào));
A.原子?????????? B.分子????????? C.元素????????? D.單質(zhì)
Ⅱ.新國(guó)標(biāo)中對(duì)水的pH的規(guī)定為6.5≤pH≤8.5,實(shí)驗(yàn)室用pH試紙測(cè)得自來水的pH=6,說明該自來水顯 酸 (填“酸”、“堿”或“中”)性,是否符合新國(guó)標(biāo) 否 (填“是”或“否”);
Ⅲ.新國(guó)標(biāo)中消毒劑由1項(xiàng)增至4項(xiàng),加入了對(duì)用臭氧、二氧化氯和氯胺消毒的規(guī)定.
①臭氧(O3)在消毒過程中轉(zhuǎn)化為氧氣,臭氧轉(zhuǎn)化為氧氣屬于 化學(xué) (填“物理”或者“化學(xué)”)變化;
②二氧化氯消毒過程中產(chǎn)生的次氯酸根離子(ClO﹣)也有消毒作用,ClO﹣中氯元素的化合價(jià)為 +1 價(jià);
③氯胺(NH2Cl)由 3 (填數(shù)字)種元素組成,用氯胺消毒時(shí),反應(yīng)的化學(xué)方程式是NH2Cl+X═NH3+HClO,其中X的化學(xué)式為 H2O .
【考點(diǎn)】自來水的生產(chǎn)過程與凈化方法;溶液的酸堿性與pH值的關(guān)系;元素的概念;化學(xué)式的書寫及意義;有關(guān)元素化合價(jià)的計(jì)算;化學(xué)變化和物理變化的判別;質(zhì)量守恒定律及其應(yīng)用.
【專題】空氣與水.
【分析】根據(jù)物質(zhì)是由元素組成的、溶液的酸堿性與pH的關(guān)系、化學(xué)變化時(shí)有新物質(zhì)生成、離子中各元素的化合價(jià)之和等于離子的化合價(jià)、以及化學(xué)反應(yīng)前后元素的種類和原子的個(gè)數(shù)不變進(jìn)行確定物質(zhì)的化學(xué)式即可.
【解答】解:Ⅰ.物質(zhì)是由元素組成的,故這里的鎘、鉛指的是元素,故填:C;
Ⅱ.實(shí)驗(yàn)室用pH試紙測(cè)得自來水的pH=6,pH小于7的溶液呈酸性,故說明該自來水顯酸性,由于對(duì)水的pH的規(guī)定為6.5≤pH≤8.5,故不符合新國(guó)標(biāo),故填:酸;否;
Ⅲ.①臭氧(O3)在消毒過程中轉(zhuǎn)化為氧氣,生成了新的物質(zhì),故臭氧轉(zhuǎn)化為氧氣屬于化學(xué)變化,故填:化學(xué);
②ClO﹣的化合價(jià)為﹣1,氧元素的化合價(jià)為﹣2,設(shè)氯元素的化合價(jià)為x,則有x+(﹣2)=﹣1,故x=+1,故填:+1;
③氯胺(NH2Cl)由氮、氫、氯三種元素組成,化學(xué)反應(yīng)前后各原子的種類和個(gè)數(shù)不變,依據(jù)反應(yīng)的化學(xué)方程式NH2Cl+X═NH3+HClO,反應(yīng)前含有1個(gè)N原子,2個(gè)H原子,1個(gè)Cl原子和X,反應(yīng)后含有1個(gè)N原子,4個(gè)H原子,1個(gè)Cl原子,1個(gè)O原子,故X中含有2個(gè)H原子和1個(gè)O原子,故其化學(xué)式為H2O,故填:3;H2O.
【點(diǎn)評(píng)】本題考查的是物質(zhì)的組成和質(zhì)量守恒的知識(shí),完成此題,可以依據(jù)已有的知識(shí)進(jìn)行.
18.如圖是甲、乙、丙三種固體物質(zhì)的溶解度曲線圖,根據(jù)該圖回答下列問題:
(1)t1℃時(shí),三種物質(zhì)的溶解度由大到小的順序是 丙>乙>甲 ;
(2)將 t2℃時(shí)甲、乙、丙三種物質(zhì)的飽和溶液降溫到t1℃,溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)最大的是 乙 ,溶質(zhì)的質(zhì)量分?jǐn)?shù)最小的是 甲 .
【考點(diǎn)】固體溶解度曲線及其作用;溶質(zhì)的質(zhì)量分?jǐn)?shù)、溶解性和溶解度的關(guān)系.
【專題】溶液、濁液與溶解度.
【分析】根據(jù)固體的溶解度曲線可以:①查出某物質(zhì)在一定溫度下的溶解度,從而確定物質(zhì)的溶解性,②比較不同物質(zhì)在同一溫度下的溶解度大小,從而判斷飽和溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)的大小,③判斷物質(zhì)的溶解度隨溫度變化的變化情況,從而判斷通過降溫結(jié)晶還是蒸發(fā)結(jié)晶的方法達(dá)到提純物質(zhì)的目的.
【解答】解:(1)通過分析溶解度曲線可知,t1℃時(shí),三種物質(zhì)的溶解度由大到小的順序是丙>乙>甲;
(2)t1℃時(shí),乙物質(zhì)的溶解度最大,甲物質(zhì)的溶解度最小,降低溫度,甲、乙物質(zhì)會(huì)析出晶體,丙物質(zhì)不會(huì)析出晶體,應(yīng)該按照t2℃時(shí)的溶解度計(jì)算,所以將 t2℃時(shí)甲、乙、丙三種物質(zhì)的飽和溶液降溫到t1℃,溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)最大的是乙,溶質(zhì)的質(zhì)量分?jǐn)?shù)最小的是甲.
故答案為:(1)丙>乙>甲;
(2)乙,甲.
【點(diǎn)評(píng)】本題難度不是很大,主要考查了固體的溶解度曲線所表示的意義,及根據(jù)固體的溶解度曲線來解決相關(guān)的問題,從而培養(yǎng)分析問題、解決問題的能力.
19.元素周期表是學(xué)習(xí)和研究化學(xué)的重要工具,它的內(nèi)容十分豐富.下表是依據(jù)元素周期表畫出的1﹣18號(hào)元素的原子結(jié)構(gòu)示意圖:
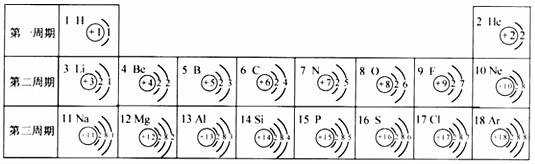
(1)核電荷數(shù)為15的元素名稱是 磷 ;核電荷數(shù)為9的元素屬于 非金屬 元素(填“金屬”或“非金屬”),在化學(xué)反應(yīng)中,該元素的原子容易 得 (填“得”或“失”)電子,與該元素化學(xué)性質(zhì)相似的另一元素是 Cl (填元素符號(hào));
(2)僅由l、7、8號(hào)元素中的三種組成的一種鹽的化學(xué)式為 NH4NO3 ;
(3)對(duì)1﹣18號(hào)元素的原子結(jié)構(gòu)示意圖進(jìn)行分析,可以發(fā)現(xiàn)許多規(guī)律,如第一周期元素的原子核外只有一個(gè)電子層.請(qǐng)?jiān)倏偨Y(jié)出其它規(guī)律,并寫出其中一條: 每一周期元素的原子的核外電子層數(shù)相同 .
【考點(diǎn)】元素周期表的特點(diǎn)及其應(yīng)用;原子結(jié)構(gòu)示意圖與離子結(jié)構(gòu)示意圖.
【專題】化學(xué)用語和質(zhì)量守恒定律.
【分析】(1)若最外層電子數(shù)≥4,則一般為非金屬元素,在化學(xué)反應(yīng)中易得電子,若最外層電子數(shù)<4,則一般為金屬元素,在化學(xué)反應(yīng)中易失去電子;元素原子的最外層電子數(shù)相同,化學(xué)性質(zhì)相似.
(2)根據(jù)題中信息結(jié)合鹽的概念進(jìn)行分析;
(3)在元素周期表中,隨原子序數(shù)的遞增,原子結(jié)構(gòu)中電子層數(shù)、最外層電子數(shù)發(fā)生規(guī)律性的變化,元素的種類(金屬、非金屬、稀有氣體).
【解答】解:(1)核電荷數(shù)為15的元素名稱是磷,核電荷數(shù)為9的元素是氟元素,屬于非金屬元素,其最外層有7個(gè)電子,在化學(xué)反應(yīng)中易得到電子,根據(jù)元素原子的最外層電子數(shù)相同,化學(xué)性質(zhì)相似可知,與該元素化學(xué)性質(zhì)相似的另一元素是為氯,故填:磷;非金屬;得;Cl;
(2)1、7、8號(hào)元素分別為氫、氮、氧,這三種可組成的鹽是硝酸銨,其化學(xué)式NH4NO3;故填:NH4NO3;
(3)每一周期元素的原子的核外電子層數(shù)相同;每一周期元素原子的最外層電子數(shù)從左到右逐漸增加;每一縱列元素原子的最外層電子數(shù)相同等.故填:每一周期元素的原子的核外電子層數(shù)相同.
【點(diǎn)評(píng)】本題難度不大,考查學(xué)生靈活運(yùn)用元素周期表中元素的信息、原子結(jié)構(gòu)示意圖及其意義進(jìn)行分析解題的能力.
三、簡(jiǎn)答題(共16分)
20.電子工業(yè)常用30%的FeCl3溶液腐蝕覆蓋有一薄層銅的絕緣板,制成印刷電路板.人們?yōu)榱藦膹U腐蝕液(含有CuCl2、FeCl2 和FeCl3)中回收銅,并重新得到FeCl3溶液,設(shè)計(jì)如下實(shí)驗(yàn)流程.
已知:2FeCl3+Fe=3FeCl2

(1)操作 ②、④的名稱是 過濾 ;
(2)上述流程中,X的化學(xué)式為 Fe ,加入過量的原因是 使溶液中的氯化鐵、氯化銅完全反應(yīng) ,步驟 ③中有關(guān)反應(yīng)的化學(xué)方程式為 Fe+2HCl═FeCl2+H2↑ ;
(3)Z為Cl2,第⑥步發(fā)生的反應(yīng)為化合反應(yīng),此反應(yīng)的化學(xué)方程式為 2FeCl2+Cl2═2FeCl3 .
【考點(diǎn)】物質(zhì)的相互轉(zhuǎn)化和制備;過濾的原理、方法及其應(yīng)用;書寫化學(xué)方程式.
【專題】物質(zhì)的制備.
【分析】(1)根據(jù)過濾可以除去不溶于水的物質(zhì)進(jìn)行分析;
(2)根據(jù)向廢液中加入過量的鐵粉時(shí),鐵能和氯化銅反應(yīng)生成氯化亞鐵和銅,鐵能和氯化鐵反應(yīng)生成氯化亞鐵進(jìn)行分析;
(3)根據(jù)氯化亞鐵能和氯氣反應(yīng)生成氯化鐵進(jìn)行分析.
【解答】解:(1)操作②、④的名稱是過濾,通過過濾把液體和不溶于水的固體分離;
(2)上述流程中,鐵能和氯化銅反應(yīng)生成氯化亞鐵和銅,鐵能和氯化鐵反應(yīng)生成氯化亞鐵,所以加入的物質(zhì)X是鐵粉,化學(xué)式為:Fe,加入過量的原因是:使溶液中的氯化鐵、氯化銅完全反應(yīng),步驟③中,加入的適量的Y是稀鹽酸,稀鹽酸能和鐵反應(yīng)生成氯化亞鐵和氫氣,化學(xué)方程式為:Fe+2HCl═FeCl2+H2↑;
(3)氯化亞鐵和氯氣反應(yīng)生成氯化鐵,化學(xué)方程式為:2FeCl2+Cl2═2FeCl3.
故答案為:(1)過濾;
(2)Fe,使溶液中的氯化鐵、氯化銅完全反應(yīng),F(xiàn)e+2HCl═FeCl2+H2↑;
(3)2FeCl2+Cl2═2FeCl3.
【點(diǎn)評(píng)】合理設(shè)計(jì)實(shí)驗(yàn),科學(xué)地進(jìn)行實(shí)驗(yàn)、分析實(shí)驗(yàn),是得出正確實(shí)驗(yàn)結(jié)論的前提,因此要學(xué)會(huì)設(shè)計(jì)實(shí)驗(yàn)、進(jìn)行實(shí)驗(yàn)、分析實(shí)驗(yàn),為學(xué)好化學(xué)知識(shí)奠定基礎(chǔ).
21.老師在指導(dǎo)學(xué)生記憶化學(xué)方程式時(shí)指出很多反應(yīng)可以歸納,如:氧化鈣、氫氧化鈣、碳酸鈣等與鹽酸反應(yīng)時(shí)生成物中都含有氯化鈣和水.同學(xué)們興趣很高,也進(jìn)行了歸納:
(1)甲物質(zhì)與稀硫酸反應(yīng)時(shí)生成物中有CuSO4和H2O,則甲物質(zhì)可以是 CuO 和 Cu(OH)2 (請(qǐng)?zhí)顚憙煞N不同類別物質(zhì)的化學(xué)式);寫出上述轉(zhuǎn)化過程中,屬于中和反應(yīng)的化學(xué)方程式 H2SO4+Cu(OH)2=CuSO4+2H2O .
(2)A﹣H都是初中常見的物質(zhì),其中D為藍(lán)色沉淀,A、E是組成元素相同的兩種氣體,F(xiàn)、H為黑色固體.他們之間轉(zhuǎn)化關(guān)系如圖(反應(yīng)條件及部分反應(yīng)物和生成物已略去)
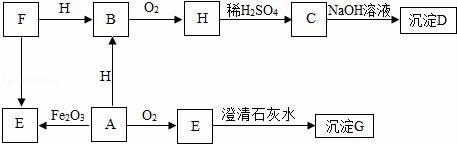
①C的化學(xué)式是 CuSO4 ;
②寫出反應(yīng)寫出反應(yīng)A![]() E的化學(xué)方程式 Fe2O3+3CO
E的化學(xué)方程式 Fe2O3+3CO![]() 2Fe+3CO2 ;
2Fe+3CO2 ;
③寫出反應(yīng)E→G的化學(xué)方程式 CO2+Ca(OH)2=CaCO3↓+H2O .
【考點(diǎn)】酸的化學(xué)性質(zhì);中和反應(yīng)及其應(yīng)用;物質(zhì)的鑒別、推斷;化學(xué)式的書寫及意義;書寫化學(xué)方程式.
【專題】框圖型推斷題;常見的酸 酸的通性.
【分析】(1)依據(jù)金屬氧化物和堿均能與酸反應(yīng)生成鹽和水的規(guī)律分析解答;
(2)依據(jù)D為藍(lán)色沉淀,則D是氫氧化銅進(jìn)行逆推,可知C是硫酸銅,H是黑色固體,則H是氧化銅,同時(shí)也可知B是銅,以此為突破口對(duì)物質(zhì)進(jìn)行推導(dǎo)分析即可;
【解答】解:(1)由于金屬氧化物和堿(碳酸鹽等也可)均能與酸反應(yīng)生成鹽和水,所以能夠生成硫酸銅和水的物質(zhì)可以為CuO和Cu(OH)2;中和反應(yīng)的要求是酸與堿生成鹽和水的反應(yīng),所以屬于中和反應(yīng)的方程式為:H2SO4+Cu(OH)2=CuSO4+2H2O;
(2)由于D為藍(lán)色沉淀,則D是氫氧化銅進(jìn)行逆推,可知C是硫酸銅,H是黑色固體,則H是氧化銅,同時(shí)也可知B是銅,A和氧化銅能夠生成銅且A是氣體,所以A是一氧化碳,一氧化碳和氧氣反應(yīng)能夠生成與之元素相同的二氧化碳,所以E是二氧化碳,二氧化碳能夠和澄清石灰水反應(yīng)能夠生成沉淀碳酸鈣G,黑色固體F能夠和H氧化銅反應(yīng)生成銅,所以F是碳;
①反應(yīng)F→B是碳的單質(zhì)與化合物氧化銅反應(yīng)生成單質(zhì)銅和化合物二氧化碳,所以該反應(yīng)屬于置換反應(yīng);
②由分析知C是CuSO4;
③反應(yīng)A![]() E化學(xué)方程式為:Fe2O3+3CO
E化學(xué)方程式為:Fe2O3+3CO![]() 2Fe+3CO2.
2Fe+3CO2.
④E→G是二氧化碳和澄清石灰水反應(yīng)生成碳酸鈣沉淀和水;反應(yīng)的化學(xué)方程式為:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案為:(1)CuO;Cu(OH)2;H2SO4+Cu(OH)2=CuSO4+2H2O;
(2)①CuSO4;②Fe2O3+3CO![]() 2Fe+3CO2;③CO2+Ca(OH)2=CaCO3↓+H2O.
2Fe+3CO2;③CO2+Ca(OH)2=CaCO3↓+H2O.
【點(diǎn)評(píng)】此題是對(duì)物質(zhì)性質(zhì)的考查,解題的關(guān)鍵是能夠?qū)ΤR娢镔|(zhì)間反應(yīng)規(guī)律的掌握.
四、實(shí)驗(yàn)題(共20分)
22.(13分)(2016?香洲區(qū)校級(jí)一模)如圖1是實(shí)驗(yàn)室常用氣體制備裝置,據(jù)圖回答問題:
(1)請(qǐng)寫出指定儀器的名稱:a 錐形瓶 ,b 集氣瓶 ;
(2)實(shí)驗(yàn)室用高錳酸鉀制氧氣的化學(xué)方程式是 2KMnO4![]() K2MnO4+MnO2+O2↑ ,應(yīng)選擇的發(fā)生裝置是 A (填字母代號(hào)),如果選用圖2裝置收集氧氣,氣體應(yīng)從 a (填“a”或“b”)端導(dǎo)入;
K2MnO4+MnO2+O2↑ ,應(yīng)選擇的發(fā)生裝置是 A (填字母代號(hào)),如果選用圖2裝置收集氧氣,氣體應(yīng)從 a (填“a”或“b”)端導(dǎo)入;
(3)某化學(xué)小組同學(xué)用20%的過氧化氫溶液和二氧化錳,并選用B裝置來制氧氣,寫出此反應(yīng)的化學(xué)方程式 2H2O2![]() 2H2O+O2↑ ;實(shí)驗(yàn)中,同學(xué)們發(fā)現(xiàn)不能得到平穩(wěn)的氧氣流,大家提出從兩個(gè)方面加以改進(jìn):
2H2O+O2↑ ;實(shí)驗(yàn)中,同學(xué)們發(fā)現(xiàn)不能得到平穩(wěn)的氧氣流,大家提出從兩個(gè)方面加以改進(jìn):
一是把發(fā)生裝置由B改為C,其理由是 注射器可以控制反應(yīng)的速度 ;
二是將過氧化氫溶液加水稀釋,溶液的稀釋需要經(jīng)過計(jì)算、量取、混勻三個(gè)步驟,如果把50g質(zhì)量分?jǐn)?shù)為20%的過氧化氫溶液稀釋成5%的過氧化氫溶液,需加水的質(zhì)量為 150 g,在稀釋過程中,除了燒杯外,還需要用到的儀器有 ①⑥ (填數(shù)字序號(hào));
①量筒? ②藥匙?? ③試管?? ④酒精燈? ⑤滴管?? ⑥玻璃棒
(4)實(shí)驗(yàn)室可用加熱氯化銨和熟石灰的固體混合物制取氨氣(NH3),
①制取氨氣應(yīng)選用的裝置是 AE (填字母代號(hào)),
②氨氣極易溶于水,氨水顯堿性.則圖3實(shí)驗(yàn)可觀察到什么現(xiàn)象? 無色變紅色,試管內(nèi)進(jìn)入一段液體 .
【考點(diǎn)】氧氣的制取裝置;一定溶質(zhì)質(zhì)量分?jǐn)?shù)的溶液的配制;氧氣的收集方法;用水稀釋改變濃度的方法;書寫化學(xué)方程式.
【專題】常見氣體的實(shí)驗(yàn)室制法、檢驗(yàn)、干燥與凈化.
【分析】錐形瓶是常用的反應(yīng)容器,集氣瓶是收集儀器的儀器;制取裝置包括加熱和不需加熱兩種,如果用雙氧水和二氧化錳制氧氣就不需要加熱,如果用高錳酸鉀或氯酸鉀制氧氣就需要加熱.氧氣的密度比空氣的密度大,不易溶于水,因此能用向上排空氣法和排水法收集.實(shí)驗(yàn)中,同學(xué)們發(fā)現(xiàn)不能得到平穩(wěn)的氧氣流,大家提出從兩個(gè)方面加以改進(jìn):一是把發(fā)生裝置由B改為C,其理由是注射器可以控制反應(yīng)的速度;有關(guān)溶液的計(jì)算要準(zhǔn)確.實(shí)驗(yàn)室可用加熱氯化銨和熟石灰的固體混合物制取氨氣,因此需要加熱;氨氣極易溶于水,密度比空氣小,因此只能用向下排空氣法收集;則圖3實(shí)驗(yàn)可觀察到的現(xiàn)象是:無色變紅色,試管內(nèi)進(jìn)入一段液體.
【解答】解:(1)錐形瓶是常用的反應(yīng)容器,集氣瓶是收集儀器的儀器,故答案為:錐形瓶;集氣瓶;
(2)如果用高錳酸鉀制氧氣就需要加熱,高錳酸鉀受熱分解生成錳酸鉀和二氧化錳和氧氣,要注意配平;如果選用圖2裝置收集氧氣,氣體應(yīng)從長(zhǎng)管進(jìn)入,因?yàn)檠鯕獾拿芏缺瓤諝獯螅还蚀鸢笧椋?KMnO4![]() K2MnO4+MnO2+O2↑;A;a;
K2MnO4+MnO2+O2↑;A;a;
(3)實(shí)驗(yàn)中,同學(xué)們發(fā)現(xiàn)不能得到平穩(wěn)的氧氣流,大家提出從兩個(gè)方面加以改進(jìn):一是把發(fā)生裝置由B改為C,其理由是注射器可以控制反應(yīng)的速度;設(shè)需加水的質(zhì)量為x,50g×20%=(50g+x)×5%,x=150g;在稀釋過程中,除了燒杯外,還需要用到的儀器有:量筒和玻璃棒,即①⑥;故答案為:2H2O2![]() 2H2O+O2↑;注射器可以控制反應(yīng)的速度;150;①⑥;
2H2O+O2↑;注射器可以控制反應(yīng)的速度;150;①⑥;
(4)實(shí)驗(yàn)室可用加熱氯化銨和熟石灰的固體混合物制取氨氣,因此需要加熱;氨氣極易溶于水,密度比空氣小,因此只能用向下排空氣法收集;則圖3實(shí)驗(yàn)可觀察到的現(xiàn)象是:無色變紅色,試管內(nèi)進(jìn)入一段液體;故答案為:AE;無色變紅色,試管內(nèi)進(jìn)入一段液體;
【點(diǎn)評(píng)】本考點(diǎn)主要考查了儀器的名稱、氣體的制取裝置和收集裝置的選擇,同時(shí)也考查了化學(xué)方程式的書寫和有關(guān)溶液的計(jì)算等,綜合性比較強(qiáng).氣體的制取裝置的選擇與反應(yīng)物的狀態(tài)和反應(yīng)的條件有關(guān);氣體的收集裝置的選擇與氣體的密度和溶解性有關(guān).本考點(diǎn)是中考的重要考點(diǎn)之一,主要出現(xiàn)在實(shí)驗(yàn)題中.
23.化學(xué)課后,化學(xué)興趣小組的同學(xué)在整理實(shí)驗(yàn)桌時(shí),發(fā)現(xiàn)有一瓶氫氧化鈉溶液沒有塞橡皮塞,征得老師同意后,開展了以下探究:
【提出問題1】該氫氧化鈉溶液是否變質(zhì)了呢?
【實(shí)驗(yàn)探究1】
實(shí)驗(yàn)操作 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
取少量該溶液于試管中,向溶液中滴加稀鹽酸,并不斷振蕩. | 有氣泡冒出. | 氫氧化鈉溶液一定變質(zhì)了. |
【提出問題2】該氫氧化鈉溶液是全部變質(zhì)還是部分變質(zhì)呢?
【猜想與假設(shè)]猜想1:氫氧化鈉溶液部分變質(zhì).? 猜想2:氫氧化鈉溶液全部變質(zhì).
【查閱資料】(1)氯化鈣溶液呈中性.
(2)氯化鈣溶液能與碳酸鈉溶液反應(yīng):CaCl2+Na2CO3═CaCO3↓+2NaCl
【實(shí)驗(yàn)探究2】
實(shí)驗(yàn)步驟 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
(1)取少量該溶液于試管中,向溶液中滴加過量的氯化鈣溶液,并不斷振蕩. | 有 白色沉淀 生成. | 說明原溶液中一定有碳酸鈉. |
(2)取步驟(1)試管中的少量上層清液,滴加酚酞溶液. | 溶液變紅色. | 說明原溶液中一定有 氫氧化鈉 . |
【實(shí)驗(yàn)結(jié)論】該氫氧化鈉溶液 部分 (填“部分”或“全部”)變質(zhì).
【反思與評(píng)價(jià)】
(1)氫氧化鈉溶液露置于空氣中容易變質(zhì),請(qǐng)寫出相關(guān)反應(yīng)的化學(xué)方程式: 2NaOH+CO2═Na2CO3+H2O .
(2)在上述【實(shí)驗(yàn)探究2】中,小明提出可用氫氧化鈣溶液代替氯化鈣溶液,你認(rèn)為該方案 不可行 (填“可行”或“不可行”).
【理解與應(yīng)用】氫氧化鈉溶液容易變質(zhì),必須密封保存.實(shí)驗(yàn)室必須密封保存的藥品還有很多,試另舉一例: 濃鹽酸具有揮發(fā)性 .
【考點(diǎn)】藥品是否變質(zhì)的探究;堿的化學(xué)性質(zhì);鹽的化學(xué)性質(zhì);書寫化學(xué)方程式.
【專題】科學(xué)探究.
【分析】由[實(shí)驗(yàn)探究2]知,(1)取少量該溶液于試管中,向溶液中滴加過量的氯化鈣溶液,溶液中的碳酸鈉會(huì)與之反應(yīng)生成碳酸鈣白色沉淀.
(2)取步驟(1)試管中的少量上層清液,滴加酚酞溶液,溶液變紅色.因碳酸鈉已完全被氯化鈣反應(yīng),所以說明原溶液中一定有氫氧化鈉.
[實(shí)驗(yàn)結(jié)論]該氫氧化鈉溶液部分變質(zhì).
[反思與評(píng)價(jià)]:(1)氫氧化鈉溶液露置于空氣中容易變質(zhì),主要是氫氧化鈉與二氧化碳反應(yīng)生成碳酸鈉和水導(dǎo)致的;
(2)在上述[實(shí)驗(yàn)探究2]中,碳酸鈉溶液和氫氧化鈉溶液都呈堿性;因此得不出氫氧化鈉部分變質(zhì)的結(jié)論.
[理解與應(yīng)用]氫氧化鈉溶液容易變質(zhì),必須密封保存.實(shí)驗(yàn)室必須密封保存的藥品還有很多,如:具揮發(fā)性的藥品、具吸水性的藥品等.
【解答】解:[實(shí)驗(yàn)探究2](1)取少量該溶液于試管中,向溶液中滴加過量的氯化鈣溶液,因碳酸鈉與氯化鈣能生成碳酸鈣沉淀,所以有白色沉淀生成,說明原溶液中一定有碳酸鈉.
(2)取步驟(1)試管中的少量上層清液,滴加酚酞溶液,溶液變紅色.溶液顯堿性,因溶液中碳酸鈉已被氯化鈣完全消耗,所以說明原溶液中一定有氫氧化鈉.從而得出[實(shí)驗(yàn)結(jié)論]該氫氧化鈉溶液部分變質(zhì).故填:
實(shí)驗(yàn)步驟 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
(1)取少量該溶液于試管中,向溶液中滴加過量的氯化鈣溶液,并不斷振蕩. | 有 白色沉淀生成. | 說明原溶液中一定有碳酸鈉. |
(2)取步驟(1)試管中的少量上層清液,滴加酚酞溶液. | 溶液變紅色. | 說明原溶液中一定有 氫氧化鈉. |
[實(shí)驗(yàn)結(jié)論]通過實(shí)驗(yàn)可以看成,該溶液中含有碳酸鈉和氫氧化鈉,是部分變質(zhì),故填:部分;
[反思與評(píng)價(jià)](1)氫氧化鈉溶液露置于空氣中容易與二氧化碳反應(yīng)生成碳酸鈉和水,相關(guān)反應(yīng)的化學(xué)方程式為:CO2+2NaOH=Na2CO3+H2O.故填:CO2+2NaOH=Na2CO3+H2O;
(2)如用酚酞試液代替稀鹽酸溶液是不行的,因?yàn)榉犹囈涸谔妓徕c溶液中也是紅色的,這樣無法確定碳酸鈉的存在,故填:不可行.
[理解與應(yīng)用]氫氧化鈉溶液容易變質(zhì),必須密封保存.實(shí)驗(yàn)室必須密封保存的藥品還有很多,如:具揮發(fā)性的藥品(濃鹽酸、氨水等)、具吸水性的藥品(濃硫酸、生石灰等)、或澄清石灰水其他合理答案均可.故填:濃鹽酸具有揮發(fā)性.
【點(diǎn)評(píng)】此題考查對(duì)一瓶沒有塞橡皮塞的氫氧化鈉溶液進(jìn)行實(shí)驗(yàn)探究過程,各環(huán)節(jié)層層相連,設(shè)計(jì)絲絲相扣,探究環(huán)節(jié)合理慎密,涉獵知識(shí)及需解答問題科學(xué)合理,仔細(xì)玩味此題,其樂無窮.
五、計(jì)算題
24.我國(guó)藥學(xué)家屠呦呦因發(fā)現(xiàn)了治療瘧疾的特效藥青蒿素(挽救了全球數(shù)百萬人的生命)于2015年10月獲得諾貝爾醫(yī)學(xué)獎(jiǎng).她在研究過程中曾關(guān)鍵性地用乙醚提取青蒿素.乙醚的化學(xué)式為C4H10O.請(qǐng)回答:
(1)每個(gè)乙醚分子中有 15 個(gè)原子,乙醚的相對(duì)分子質(zhì)量為 74 ;
(2)乙醚(C4H10O)中碳、氧元素質(zhì)量比為 3:1 ;
(3)乙醚(C4H10O)中碳元素的質(zhì)量分?jǐn)?shù)是 64.9% (精確到0.1%).
【考點(diǎn)】元素的質(zhì)量分?jǐn)?shù)計(jì)算;相對(duì)分子質(zhì)量的概念及其計(jì)算;元素質(zhì)量比的計(jì)算.
【專題】化學(xué)式的計(jì)算;有關(guān)化學(xué)式的計(jì)算.
【分析】(1)根據(jù)乙醚化學(xué)式的意義以及相對(duì)分子質(zhì)量的計(jì)算方法來分析;
(2)根據(jù)化合物中各元素質(zhì)量比=各原子的相對(duì)原子質(zhì)量×原子個(gè)數(shù)之比,進(jìn)行分析;
(3)根據(jù)化合物中元素質(zhì)量分?jǐn)?shù)的計(jì)算方法來分析.
【解答】解:(1)由乙醚的化學(xué)式為C4H10O可知,每個(gè)乙醚分子中含有4個(gè)碳原子、10個(gè)氫原子和1個(gè)氧原子,共有15個(gè)原子;乙醚的相對(duì)分子質(zhì)量=12×4+1×10+16=74;故填:15;74;
(2)乙醚中碳、氧元素的質(zhì)量比為(12×4):(16×1)=3:1;故填:3:1;
(3)乙醚(C4H10O)中碳元素的質(zhì)量分?jǐn)?shù)是![]() ×100%≈64.9%;故填:64.9%.
×100%≈64.9%;故填:64.9%.
故答案為:
(1)15,74;(2)3:1;(3)64.9%.
【點(diǎn)評(píng)】本題難度不大,考查同學(xué)們結(jié)合新信息、靈活運(yùn)用化學(xué)式的含義與有關(guān)計(jì)算進(jìn)行分析問題、解決問題的能力.
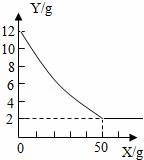
25.銅仁市地處武陵山區(qū),石灰石資源豐富,某課外小組同學(xué)取該樣品12.0g于燒杯中,向盛有樣品的燒杯中加入足量一定溶質(zhì)質(zhì)量分?jǐn)?shù)的稀鹽酸溶液充分反應(yīng),所用稀鹽酸質(zhì)量(用X表示)和燒杯中剩余固體質(zhì)量(用Y表示)如圖所示(石灰石的主要成分是碳酸鈣,雜質(zhì)不溶于水也不與酸反應(yīng)),請(qǐng)回答下列問題:
(1)石灰石中碳酸鈣的質(zhì)量是多少?
(2)充分反應(yīng)后共生成多少二氧化碳?
(3)所用稀鹽酸的溶質(zhì)質(zhì)量分?jǐn)?shù)是多少?
【考點(diǎn)】根據(jù)化學(xué)反應(yīng)方程式的計(jì)算;有關(guān)溶質(zhì)質(zhì)量分?jǐn)?shù)的簡(jiǎn)單計(jì)算.
【專題】化學(xué)計(jì)算;綜合計(jì)算(圖像型、表格型、情景型計(jì)算題).
【分析】首先正確寫出方程式,然后根據(jù)題干內(nèi)容分析得出反應(yīng)后剩余固體即為雜質(zhì),質(zhì)量差即為碳酸鈣的質(zhì)量結(jié)合化學(xué)方程式可以計(jì)算生成二氧化碳?xì)怏w的質(zhì)量和所用稀鹽酸的溶質(zhì)質(zhì)量,就可以進(jìn)一步求出所用稀鹽酸的溶質(zhì)質(zhì)量分?jǐn)?shù)是.
【解答】解:(1)石灰石中碳酸鈣的質(zhì)量是12g﹣2g=10g;
(2)設(shè)生成二氧化碳的質(zhì)量為x,所用稀鹽酸的溶質(zhì)質(zhì)量為y,
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
100??? 73??????????? 44
10g??? y???????????? x
![]()
x=4.4g
y=7.3g
(3)所用稀鹽酸的溶質(zhì)質(zhì)量分?jǐn)?shù)是![]() ×100%=14.6%;
×100%=14.6%;
答:(1)石灰石中碳酸鈣的質(zhì)量是10g;
(2)生成二氧化碳的質(zhì)量為4.4g.
(3)所用稀鹽酸的溶質(zhì)質(zhì)量分?jǐn)?shù)是14.6%.
【點(diǎn)評(píng)】解答此題的依據(jù)是根據(jù)方程式找準(zhǔn)已知量,未知量關(guān)系,列比例式求解即可.

孔乙己是貧困潦倒的知識(shí)分子。在書中,孔乙己是一個(gè)知識(shí)分子,滿口“之乎者也”,但是他很窮,還竊書,說過“讀書人的事,怎么能叫竊,”被人嘲笑,他...

自然界產(chǎn)生氧氣的化學(xué)方程式:光合作用的反應(yīng)式為6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反應(yīng)和暗反應(yīng)兩個(gè)過程。需要具備光...

有的高校沒有條件,只要學(xué)業(yè)水平成績(jī)都合格就可以,比如中國(guó)科學(xué)院大學(xué)。有的需要平常學(xué)習(xí)考試成績(jī),比如北京外國(guó)語大學(xué)要求高三第一學(xué)期期末成績(jī)?cè)谌?..

在四則運(yùn)算中,表示計(jì)算順序,在小括號(hào)之后、大括號(hào)之前;表示兩個(gè)整數(shù)的最小公倍數(shù);表示取未知數(shù)的整數(shù)部分;在函數(shù)中,表示函數(shù)的閉區(qū)間;在線性代...

濟(jì)南開設(shè)的最好的職高學(xué)校有:濟(jì)南方信集團(tuán)職業(yè)高中、濟(jì)南公共交通職業(yè)高中。濟(jì)南市公共交通職業(yè)高級(jí)中學(xué)是由濟(jì)南市公共交通總公司承辦,業(yè)務(wù)屬濟(jì)南市...

實(shí)然:是說事物實(shí)際上就是這樣的,但不同于現(xiàn)實(shí)性(現(xiàn)實(shí)性指其有合理性和客觀性);應(yīng)然:就是應(yīng)該是怎么樣的意思,比如說這件事,就應(yīng)該是那樣的結(jié)果...

地中海氣候一種夏季炎熱干燥、冬季溫和多雨,雨熱不同期的氣候類型。地中海氣候冬季受西風(fēng)帶控制,鋒面氣旋頻繁活動(dòng),氣候溫和,最冷月的氣溫在4-1...

堿石灰,又稱鈉石灰,堿石灰是白色或米黃色粉末,疏松多孔,是氧化鈣(CaO,大約75%),水(H?O,大約20%),氫氧化鈉(NaOH,大約3...