 江蘇省淮安市2017初中畢業暨中等學校招生文化統一考試
江蘇省淮安市2017初中畢業暨中等學校招生文化統一考試
化學試題
歡迎參加中考,相信你能成功!請先閱讀以下幾點注意事項:
1. 試卷分為第一部分、第二部分兩部分,共6頁,全卷60分,考試時間60分鐘。
2. 第一部分每小題選出答案后,請用2B鉛筆把答題卡上對應題目煩人答案標號涂黑。如需改動,先用橡皮擦干凈后,再選涂其它答案,答案寫在試卷上無效。
3.做第二部分時,用0.5毫米黑色墨水簽字筆,將答案寫在答題卡上相應題號后的橫線上,答案寫在本試卷上或答題卡上規定區域以外無效。
4. 考試結束后,將本試卷和答題卡一并交回。
5. 可![]() 能用到的相對原子質量:
能用到的相對原子質量:
H-1N-14![]() O-16Na-23Mg-24S-32Cl-35.5K-39Fe-56
O-16Na-23Mg-24S-32Cl-35.5K-39Fe-56
第一部分(選擇題 共20分)
一、選擇題(本題共10小題,每小題2分,共20分。每小題只有一個選項符合題意)
1. 下列變化中,屬于化學變化的是
A. 粉筆折斷![]() B. 棉紗織布 C. 木材燃燒D. 汽油揮發
B. 棉紗織布 C. 木材燃燒D. 汽油揮發
2. 下列實驗操作錯誤的是
![]()
![]()
![]()
![]()
A B C D
3. 下列生活中常見物質與水混合,能![]() 形成溶液的是
形成溶液的是
A. 牙膏B. 蔗糖C. 面粉D. 豆油
4. 下列做法會危害人體健康的是
A. 飲用低溫滅菌牛奶B. 食用新鮮蔬菜水果
C. 用小蘇打做發酵粉D. 用甲醛浸泡水產品
5. 某博物館藏有一柄古代鐵劍,為防止其生銹,下列做法合理的是
A. 定期用清水沖洗,除去灰塵B. 放于體驗區,讓觀眾觸摸
C. 用鹽水除去鐵劍上的銹斑D. 放在充滿氮氣的展覽柜中
6. 焦亞硫酸鈉在食品加工中常用作防腐劑、漂白劑和疏松劑。焦亞硫酸鈉(Na2S2O6)中硫元素的化合價為
A. -2 B. +3C.![]() +4 D. +5
+4 D. +5
7. 下列有關水的說法正確的是
A. 水中加入固體硝酸銨可降低溶![]() 液溫度
液溫度
B. 通過活性炭的吸附可使硬水變為軟水
C. 為保護水資源,禁止使用化肥和農藥
D. 無色透明的深層地下水屬于純凈物
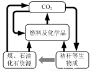
8. 題8圖是我國《可再生資源法》倡導的碳資源的轉化與循環利用示意圖。下列做法與該圖體現的理念不符的是
A. 將秸稈加工轉化為酒精燃料
B. 二氧化碳作為原料生產尿素
C. 過度開采煤、石油作為燃料
D. 將石油精煉,制備合成材料
9. 下列實驗方案不能達到實驗目的的是
選項 | 實驗目的 | 實驗方案 |
A | 區別聚乙烯與聚氯乙烯 | 分別將兩種塑料灼燒,聞氣味 |
B | 比較銅與銀的金屬活動性強弱 | 將銅和銀分別放入鹽酸中,觀察現象 |
C | 區別天然氣與一氧化碳 | 分別點燃兩種氣體,檢驗燃燒產物 |
D | 判斷溫度對溶解速率的影響 | 對比高錳酸鉀 |
10. 下列四個圖像中,能正確反映對應變化關系的是
|
|
|
|
A. 用CuFe2O4-x做催化劑,光分解水制氫氣與氧氣 | B. 向氯化鈉的飽和溶液中加入硝酸鉀 | C. 向混有少量硫酸的硫酸銅溶液中加入氫氧化鈉溶液 | D. 向一定質量的碳酸鈉溶液中加水 |
第二部分 (非選擇題 共40分)
二、填充與簡答題(本題共5小題,共18分)
11.(3分)用符合要求的物質的序號填空。
①生石灰②鹽酸 ③石墨 ④碘酒
(1)可用于傷口消毒的是▲。
(2)可用于制作鉛筆芯的是▲。
(3)可用作食品干燥劑的是▲。
12.(4分)質量守恒定律的發現對化學的發展作出了巨大貢獻。

(1)為驗證質量守恒定律,小華設計如題12-1圖所示裝置進行實驗。
實驗時,先將裝有藥品的裝置放在天平上,添加砝碼,移動游碼至天平平衡(如題12-1圖所示),然后取下裝置,用針筒向錐形瓶中注入少量稀鹽酸,反應后再將裝置放置于天平上,觀察到▲ ![]() ,從而驗證了質量守恒定律。若將錐形瓶改為燒杯,則不能驗證質量守恒定律,原因是▲。
,從而驗證了質量守恒定律。若將錐形瓶改為燒杯,則不能驗證質量守恒定律,原因是▲。
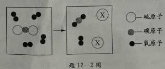
(2)某反應的微觀示意圖如題12-2圖所示。
①X的化學式是▲。
②根據上述微觀示意圖,可得出化學反應遵循質量守恒定律的本質原因是▲。
13.(4分)如題13圖所示是四種物質的溶解度曲線圖,請回答下列問題。

(1)在60℃時,四種物質中溶解度最大的是▲。
(2)將40℃時氯化鉀的不飽和溶液,保持溶液溫度不變,
制成飽和溶液,可行的方法有▲(舉1例)。
(3)在t℃時,將30g氯化銨加入50g水中,充分溶解,
所得溶液質量分數為▲ (精確到0.1%)。
(4)向飽和食鹽水中加入足量的碳酸氫銨固體,會有溶解度較小的碳酸氫鈉晶體析出,該反應的化學方程式是NaCl+NH4HCO3 =NaHCO3↓+NH4Cl,請根據以上信息和題13圖中物質的溶解度曲線,簡述以硫酸銨固體為原料制取較純硫酸鉀晶體的方法:▲。
14.(4分)我國化學家傅鷹教授有一句名言“科學只給我們知識,而歷史卻給我們智慧”在化學學習中,了解知識的發展歷程,可以促進我們正確理解科學本質。
(1)我國西漢時期就有“曾青得鐵則化為銅”的記載,期中蘊涵的濕法冶銅原理為▲(用化學方程式表示)。
(2)火藥起源于唐朝。為使煙火產生耀眼的白光,可在其火藥中加入▲(填一種金屬名稱)。
(3)十八世紀,化學家們研究發現某些金屬與酸反應能生成一種氣體,該氣體被喻為“會制造水的物質”,對上述反應原理的認識加快了推翻燃素學說的進程。該氣體在空氣中燃燒制造水的化學方程式是 ▲ 。
(4)現代以來,人們對金屬的認識不斷深入,助推多種新材料的研制與使用。2017年5月5日我國首架試飛成功的大型客機C919使用了多種新材料,其中有鋰鋁合金,在飛機制造中使用該材料說明其具有的有點有▲ (填序號)。
①硬度大 ②密度小③易導電④耐腐蝕
![]()
15.(3分)X、Y、Z、M、Q為生活中常見物質。Q為單質,其余為化合物,X為呼吸作用的產物,M為光合作用的產物,Z常溫下為液體。各物質之間的轉化關系如題15圖所示(部分反應物、生成物、轉化關系及反應條件未標出![]() ),回答下列問題:
),回答下列問題:
(1)M屬于▲ (填“無機物”或“有機物”)。
![]() (3)若Y屬于鹽類物質,則X Y可能發生的化學反應方程式是 ▲ (舉1例)。
(3)若Y屬于鹽類物質,則X Y可能發生的化學反應方程式是 ▲ (舉1例)。
三、實驗與探究題(本題共3小題,共16分)
16.(4分)根據題16圖回答下列問題:
(1)圖B中標有序號①的儀器名稱是▲。
(2)組裝好氣體發生裝置后,先應該檢查裝置的▲ ,然后再添加藥品。
(3)欲收集密度比空氣大的氣體,應該選擇的裝置是▲ (填序號)。
(4)實驗室用石灰石與稀鹽酸反應制取二氧化碳的化學方程式是▲。
17.(6分)小文同學利用長柄W形玻璃管,完成了課本上多個化學實驗。![]()
1)燃燒條件的探究與空氣中氧氣含量的粗略測定
①燃燒條件的探究:在如題17-1圖所示裝置(省略夾持儀器,下同)中,向W形玻璃管中放入足量紅磷和白磷,塞好橡皮塞,關閉活塞,然后將其放入80℃的熱水中,觀察到紅磷![]() 不燃燒而白磷燃燒,說明可燃物發生燃燒應具備的條件是▲。
不燃燒而白磷燃燒,說明可燃物發生燃燒應具備的條件是▲。
②空氣中氧氣含量的粗略測定:為減小測量誤差,待火焰熄滅后,將玻璃管 ▲ ,再打開活塞。
(2)一氧化碳與氧化鐵反應
①甲酸(HCOOH)在熱濃硫酸的作用下,分解生成一氧化碳和水,該反應的化學方程式是▲。
② 實驗時,A處可以觀察到的現象是▲。
(3)探究微粒的性質
向玻璃管左端加入試劑X,觀察到無色酚酞試液變紅,濕潤的紅色石蕊試紙變藍,試劑X可能是▲ ,該裝置的優點有 ▲ (答1點)。
18.(6分)氯化鎂是一種重要的化工原料,同學們在實驗室對其開展了系列研究。
課題1:選擇制取氯化鎂的原料
【查閱資料】
①全球海水中含有的鹽類總質量為5億億噸,其中含有的各種離子占鹽類總質量的百分含量如下表所示:
離子 | Cl— | Na+ | Mg2+ | Ca2+ | K+ | 其他 |
含量 | 55.06% | 30.61% | 3.69% | 1.15% | 1.10% | …… |
②工業生產中海水或鹵水(海水曬鹽后的剩余溶液)都可以作為制取氯化鎂的原料![]() 。
。
【交流討論】
同學們經討論,一致選擇鹵水用于實驗室制取氯化鎂。你認為他們的理由是 ▲ 。課題2:由鹵水制取氯化鎂
同學們設計如題18圖所示方案,從鹵水中制取氯化
(1)溶液X的名稱是 ▲ 。
(2)部分同學認為上述制取方案不夠完善,在“過濾”操作后缺少“洗滌”操作,從而導致制取的氯化鎂不純,可能混有的雜質是 ▲ 。
課題3:測定氯化鎂產品的純度(氯化鎂的質量分數)
同學們設計如下實驗方案對制得的氯化鎂進行純度測定。
【實驗步驟】
①稱取9.5g氯化鎂樣品,放于燒杯中,加足量的水溶解,形成溶液;
②向上述溶液中加入90g質量分數為10%的氫氧化鈉溶液;
③充分反應后,過濾;
④……
⑤向所得溶液中加入幾滴無色酚酞試液,溶液變紅,再逐滴加入10%稀硫酸(密度為1.07g·mL—1),并 ▲ ,當觀察到溶液恰好褪色且30s內紅色不復現,停止加入稀硫酸;
⑥計算氯化鎂樣品的純度。
【問題討論】
(1)為計算出氯化鎂樣品的純度,除上述數據外,實驗還需測量的數據是 ▲ 。
(2)若缺少步驟④,則會導致氯化鎂純度測定不準確,步驟④的操作是 ▲ 。
四、計算題(本題共1小題,共6分)
19.(6分)高鐵酸鈉(Na2FeO4)是一種高效多功能水處理劑,工業上常采用次氯酸鈉(NaClO)氧化法生產,反應原理用化學方程式表示為:
3NaClO + 2Fe(NO3)3 + 10NaOH = ![]() 2Na2FeO4↓+3NaCl +6NaNO3 + 5H2O
2Na2FeO4↓+3NaCl +6NaNO3 + 5H2O
(1)在Fe(NO3)3中,鐵元素和氮元素的質量比為▲ (填最簡比)。
(2)縣稱取44.7g次氯酸鈉,最多能制得高鐵酸鈉的質量是多少?(列式計算)
溫馨提示:NaClO的相對分子質量為74.5;Na2FeO4的相對分子質量為166。
祝賀你順利完成答題,可別忘了認真檢查哦!
江蘇省淮安市2017年初中畢業暨中等學校招![]() 生文化考試統一試卷
生文化考試統一試卷
化學試題參考答案及評分標準
一、選擇題(每小題2分,共20分)
題號 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | C | A | B | D | D | C | A | C | B | D |
二、填空與簡答題(每空1分,共18分)
11.(1)④(2)③(3)①
12.(1)天平平衡或指針指在分度盤的中央或質量為72.6g或指針左右等幅擺動;裝置沒有密閉或氣體逸出了
(2)①SO2 ②化學反應前后,原子不變或原子數目和種類不變
13.(1)硫酸銨(或(NH4)2SO4)
(2)加溶質氯化鉀至不再溶解為止(或恒溫蒸發至晶體析出) (3)28.6%
(4)向熱的飽和硫酸銨溶液中加足量的氯化鉀,有大量固體析出,趁熱過濾(或向熱的飽和氯化鉀溶液中加足量硫酸銨,有固體析出,降溫至20℃左右,過濾)
14.(1)Fe + CuSO4 = FeSO4 + Cu(2)鎂
(3)2H2 + O2 ![]() 2H2O(4)①②④(多選、少選或選錯均不給分)
2H2O(4)①②④(多選、少選或選錯均不給分)
15.(1)有機物 (2)O2 (3)CO2+Ca(OH)2 =CaCO3↓+H2O等(其它合理答案也得分)
三、實驗與探究題(每空1分,共16分)
16.(1)分液漏斗(2)氣密性(或是否漏氣)(3)D(4)CaCO3+2HCl =CaCl2+H2O+CO2↑
![]() 17.(1)①可燃物的溫度必須達到著火點②冷卻至室溫
17.(1)①可燃物的溫度必須達到著火點②冷卻至室溫
(2)①HCOOH H2O+CO↑②紅棕色粉末變成黑色粉末
(3)濃氨水 裝置簡單或節約藥品或環保(其它合理答案也得分)
18. 課題1鹵水中氯化鎂含量高 課題2 (1)鹽酸(2)氯化鈉、氯化鉀和氯化鈣(三者缺一不得分,也可混有其他合理雜質)
課題3 【實驗步驟】⑤玻璃棒攪拌或搖晃或振蕩
【問題討論】①稀硫酸反應最后的體積或稀硫酸反應前后的質量,或加入酚酞后混合溶液質量與反應后混合溶液質量或稀硫酸的體積等。
②用水充分洗滌濾渣,并將洗![]() 滌液與濾液合并
滌液與濾液合并
四、計算題(6分)
19.(1)4:3 (2分)
(2)解:設高鐵酸鈉的質量為X
3NaClO + 2Fe(NO3)3 + 10NaOH = 2Na2FeO4↓+3NaCl +6NaNO3 + 5H2O
223.5332
44.7gX (1分)
(1分)
X=66.4g (2分)
答:最多可得到高鐵酸鉀的質量為66.4g。

孔乙己是貧困潦倒的知識分子。在書中,孔乙己是一個知識分子,滿口“之乎者也”,但是他很窮,還竊書,說過“讀書人的事,怎么能叫竊,”被人嘲笑,他...

自然界產生氧氣的化學方程式:光合作用的反應式為6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反應和暗反應兩個過程。需要具備光...

有的高校沒有條件,只要學業水平成績都合格就可以,比如中國科學院大學。有的需要平常學習考試成績,比如北京外國語大學要求高三第一學期期末成績在全...

在四則運算中,表示計算順序,在小括號之后、大括號之前;表示兩個整數的最小公倍數;表示取未知數的整數部分;在函數中,表示函數的閉區間;在線性代...

濟南開設的最好的職高學校有:濟南方信集團職業高中、濟南公共交通職業高中。濟南市公共交通職業高級中學是由濟南市公共交通總公司承辦,業務屬濟南市...

實然:是說事物實際上就是這樣的,但不同于現實性(現實性指其有合理性和客觀性);應然:就是應該是怎么樣的意思,比如說這件事,就應該是那樣的結果...

地中海氣候一種夏季炎熱干燥、冬季溫和多雨,雨熱不同期的氣候類型。地中海氣候冬季受西風帶控制,鋒面氣旋頻繁活動,氣候溫和,最冷月的氣溫在4-1...

堿石灰,又稱鈉石灰,堿石灰是白色或米黃色粉末,疏松多孔,是氧化鈣(CaO,大約75%),水(H?O,大約20%),氫氧化鈉(NaOH,大約3...